код мкб фибрилляция и трепетание предсердий
Фибрилляция и трепетание предсердий (I48)
Тип I трепетания предсердий
Тип II трепетания предсердий
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Код мкб фибрилляция и трепетание предсердий
МКБ 10: I48
Год утверждения (частота пересмотра): 2016 (7-10 лет)
ID: 382
Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и электростимуляции.
Общество специалистов по неотложной кардиологии
Ключевые слова
Список сокращений
ААП – антиаритмические препараты
АД – артериальное давление
ЕОК – Европейское общество кардиологов
ИБМ – ишемическая болезнь мозга
ИБС – ишемическая болезнь сердца
ИМ – инфаркт миокарда
ИПН – ингибиторы протонного насоса
КТ – компьютерная томография
ЛЖ – левый желудочек сердца
МРТ – магнитно-резонансная томография
НЖТ – наджелудочковая тахикардия
РФ – Российская Федерация
СКФ – скорость клубочковой фильтрации
ССЗ – сердечно-сосудистые заболевания
ФК – функциональный класс
ХСН – хроническая сердечная недостаточность
Термины и определения
1. Краткая информация
1.1. Определение
Трепетание предсердий относится к предсердным тахикардиям, обусловленным циркуляцией волны возбуждения по топографически обширному контуру (т.н. «макро-реэнтри»), как правило, вокруг крупных анатомических структур в правом или левом предсердии [2,3]. По ЭКГ ТП представляет собой правильный высокоамплитудный предсердный ритм с высокой частотой (обычно от 250 до 400 в минуту) и отсутствием чёткой изоэлектрической линии между предсердными комплексами (волнами F) хотя бы в одном отведении ЭКГ. Волны F при ТП чаще всего имеют т.н. пилообразный характер хотя бы в одном отведении ЭКГ.
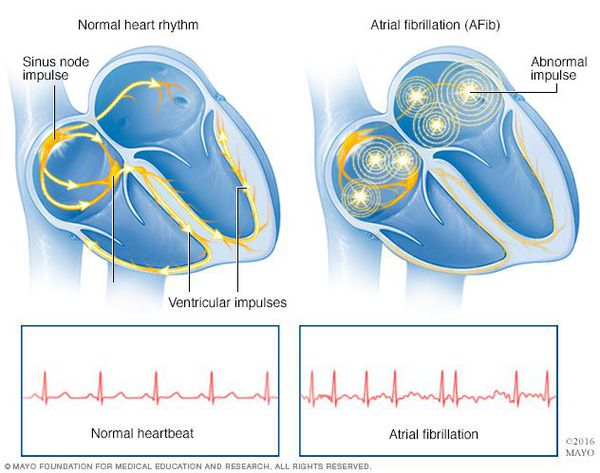
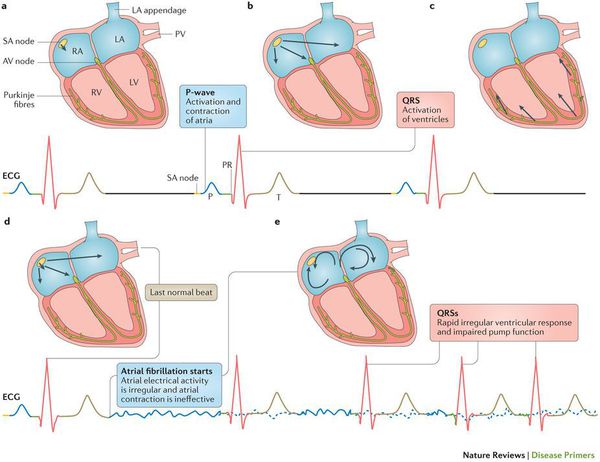
Фибрилляция предсердий представляет собой наджелудочковую тахиаритмию, характеризующуюся хаотической электрической активностью предсердий с высокой частотой (как правило, от 300 до 700 в минуту) и нерегулярным ритмом желудочков (при условии отсутствия полной АВ-блокады). Характерными ЭКГ-признаками ФП являются: отсутствие зубцов Р, наличие разноамплитудных, полиморфных волн ff, переходящих одна в другую без чёткой изолинии между ними, а также абсолютная хаотичность и нерегулярность ритма желудочков 2. Последний признак не регистрируется в случаях сочетания ФП и АВ-блокады III степени (при т.н. феномене Фредерика). Основные диагностические признаки ФП и ТП в сравнении с другими формами НЖТ представлены в ПРИЛОЖЕНИИ Д-2.
1.2. Этиология и патогенез
Для возникновения устойчивых ФП и ТП необходимо наличие трёх составляющих: 1) пусковых, т.н. триггерных факторов аритмии, 2) аритмогенного субстрата аритмии, обеспечивающего самостоятельное поддержание аритмии, а также 3) индивидуальных модулирующих влияний, повышающих восприимчивость аритмогенного субстрата к триггерным факторам.
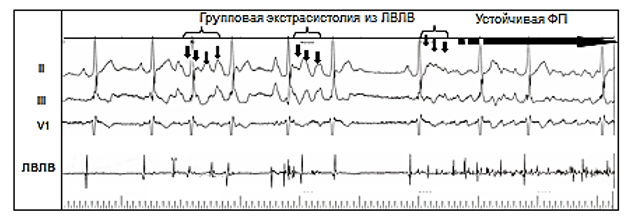
В подавляющем большинстве случаев (95%) триггерным фактором ФП является патологическая высокочастотная электрическая активность в устьях легочных вен, отражением которой на ЭКГ является частая ранняя предсердная экстрасистолия (по типу «Р на Т», см. рис.1) и/или пробежки предсердной тахикардии (как монофокусной, так и хаотической).
Рис. 1. Возникновение приступа фибрилляции предсердий вследствие частой эктопической активности из устья левой верхней легочной вены.
Обозначения: ЛВЛВ – электрограмма из устья левой верхней легочной вены; A – осцилляции предсердий. Индексом 1 обозначены электрические сигналы синусового происхождения, индексом 2 – электрические сигналы эктопии из ЛВЛВ.
Более редкими тригерными факторами ФП являются экстрасистолы из полых вен, а также предсердные экстрасистолы. Электрофизиологическими механизмами очаговой активности лёгочных и полых вен является триггерная активность и повторный вход возбуждения (re-entry) в мышечных структурах, выстилающих места их впадений в предсердия. При проведении ЭФИ приступы ФП и, особенно, ТП могут быть вызваны электростимуляцией предсердий [4,5].
Для возникновения ТП также требуется предсердная экстрасистолия, однако у пациентов с отсутствием сочетанной ФП триггеры обычно локализуются вне лёгочных вен. Аритмогенный субстрат ТП представляет из себя цепь макро-реэнтри (протяжённую петлю циркуляции возбуждения) в правом и/или левом предсердиях, возникшую вследствие нарушения процессов проведения электрического возбуждения по предсердному миокарду. Критическими компонентами цепи макро-реэнтри ТП являются наличие протяжённого анатомического барьера, вокруг которого возможна циркуляция импульсов, а также зоны замедленного проведения в одном или нескольких участков этой цепи, позволяющей фронту волны возбуждения замедлять ход и не наталкиваться на рефрактерный участок предсердий, следующей за хвостовой частью волны реэнтри [3,6-8].
Аритмогенный субстратФП представляет собой структурно и функционально изменённый (ремоделированный) миокард предсердий, обеспечивающий стойкое самостоятельное поддержание хаотической электрической активности предсердий. Под ремоделированием понимают совокупность патологических процессов, возникающих в предсердиях в ответ на возникновение ФП или/и в результате действия известных этиологических факторов. Ремоделирование начинается с нарушения ионных клеточных механизмов формирования импульса и заканчивается структурно-функциональной деградацией предсердного миокарда и атриомегалией. Основными структурными изменениями миокарда предсердий, предрасполагающими к возникновению субстрата ФП, являются фиброз, воспаление, апоптоз и гипертрофия кардиомиоцитов. Функциональные нарушения в предсердном миокарде включают в себя возникновение неоднородности скоростей проведения импульсов в разных направлениях, а также дисперсию процессов реполяризации в предсердном миокарде. Прогрессирование ФП и резистентность аритмии к лекарственному и интервенционному лечению, как правило, определяется выраженностью процессов ремоделирования предсердий. В настоящее время рассматриваются две альтернативные электрофизиологические гипотезы самоподдержания ФП: 1) наличие одного или нескольких высокочастотных роторов в предсердиях или лёгочных венах с постоянно меняющимся характером проведения импульсов на окружающий миокард предсердий; 2) циркуляция множественных волн микро-реэнтри в предсердиях по неопределенному, случайному пути.
Наиболее частым модулирующим влиянием, способствующим активации «спящего» аритмогенных субстратов ФП и ТП в ответ на действие триггерного фактора, является дисбаланс вегетативных влияний на миокард предсердий. В зависимости от характера нарушений автономной регуляции работы сердца выделяют т.н. «вагусную» форму мерцательной аритмии (аритмия возникает преимущественно во время сна или после переедания, при резких наклонах или поворотах туловища, а также любых других факторах, усиливающих парасимпатические влияния на сердце), а также т.н. «гиперадренергическую» форму мерцательной аритмии (ФП/ТП возникают преимущественно в момент физической нагрузки, при стрессе, резком испуге и других состояниях, сопровождающихся повышением симпатических влияний на сердце). В качестве других модулирующих влияний могут выступать нарушения электролитного обмена (гипокалиемия), преходящая ишемия миокарда и проаритмическое действие лекарственных препаратов 2.
1.3. Эпидемиология
Фибрилляция предсердий – самая распространённая тахиаритмия в клинической практике. В популяции её частота достигает 1-2% 2. По данным, представленным в рекомендациях европейского общества кардиологов в 2012 году, в Европе в настоящее время насчитывается более 6 миллионов человек, страдающих ФП, а в ближайшие 50 лет их число, как минимум, удвоится [3,10]. Трепетание диагностируется существенно реже, чем ФП, приблизительно в 7-10% случаев всех суправентрикулярных тахиаритмий. Хорошо известно, что частота ФП и ТП увеличивается с возрастом, так среди лиц старше 80 лет почти 10% страдают ФП. Примерно треть всех госпитализаций по поводу аритмий приходится на ФП и ТП. Анализ 63 589 больных со стабильными проявлениями атеротромбоза, включёнными во всемирный регистр REACH, показал, что у данной категории пациентов частота ФП составляет 10,7%. У мужчин ФП и ТП обнаруживается примерно в 4-5 раз чаще, чем у женщин.
1.4. Кодирование по МКБ 10
Фибрилляция и трепетание предсердий неуточненное
Рубрика МКБ-10: I48.9
Содержание
Определение и общие сведения [ править ]
Синонимы: мерцательная аритмия
Этиология и патогенез [ править ]
Самые частые причины мерцательной аритмии — ревматические пороки сердца, артериальная гипертония, ИБС и тиреотоксикоз. Кроме того, она может наблюдаться при инфаркте миокарда, ХОЗЛ, ТЭЛА, гипокалиемии, перикардите, дефектах межпредсердной перегородки, сердечной недостаточности, алкоголизме. Иногда причину ее установить не удается (идиопатическая мерцательная аритмия). Во всех случаях необходимо проверить электролиты крови и функцию щитовидной железы (у пожилых мерцательная аритмия может быть единственным проявлением тиреотоксикоза). В зависимости от предполагаемой причины проводят дополнительные исследования: измеряют активность сердечных изоферментов (инфаркт миокарда), исследуют газы артериальной крови (гипоксемия), проводят вентиляционно-перфузионную сцинтиграфию (ТЭЛА), ЭхоКГ (органические поражения сердца) и нагрузочные пробы (ИБС). ЭКГ — см. гл. 5, п. II.Б.2.
А. Отдельные формы мерцательной аритмии:
1. брадисистолическая форма: низкая ЧСС нередко обусловлена синдромом слабости синусового узла; после успешной кардиоверсии может развиться синоатриальная или АВ-блокада высокой степени. Перед кардиоверсией таким больным устанавливают зонд-электрод для временной эндокардиальной ЭКС;
2. мерцательная аритмия с правильным ритмом желудочков: часто служит проявлением гликозидной интоксикации, на фоне которой возникает полная АВ-блокада с замещающим АВ-узловым ритмом. Электрическая кардиоверсия противопоказана;
3. мерцательная аритмия с широкими комплексами QRS: причина появления широких комплексов QRS — либо блокада ножки пучка Гиса, либо синдром WPW.
Клинические проявления [ править ]
Фибрилляция и трепетание предсердий неуточненное: Диагностика [ править ]
Дифференциальный диагноз [ править ]
Фибрилляция и трепетание предсердий неуточненное: Лечение [ править ]
1. В отсутствие жалоб или их слабой выраженности, особенно при нормальной функции левого желудочка, проводят амбулаторное лечение:
а. при ЧСС > 100 мин –1 : прием блокаторов АВ-проведения и варфарина (поддерживать МНО на уровне 2,0—3,0) в течение 3 нед, затем — госпитализация для плановой электрической или медикаментозной кардиоверсии (см. гл. 6, п. IV.Б.3.в);
б. при ЧСС –1 : варфарин в течение 3 нед (поддерживать МНО на уровне 2,0—3,0), затем — госпитализация для плановой электрической или медикаментозной кардиоверсии;
в. при кратковременных, хорошо переносимых пароксизмах бывает достаточно покоя и седативной терапии.
2. Выраженные жалобы, нарушения гемодинамики, сопутствующая дисфункция левого желудочка требуют госпитализации. Тактика следующая:
а. длительность пароксизма б. длительность пароксизма > 2 сут: снижение ЧСС, назначение антикоагулянтов (см. гл. 6, п. IV.Б.3.в), выписка, через 3 нед — повторная госпитализация для плановой электрической или медикаментозной кардиоверсии.
3. Восстановление синусового ритма
1) Если пароксизм длится 2) Если пароксизм длится > 2 сут: варфарин по крайней мере в течение 3 нед (поддерживать МНО на уровне 2,0—3,0) до и после плановой электрической или медикаментозной кардиоверсии. Антикоагулянтная терапия уменьшает риск тромбоэмболий. Есть сообщение о нецелесообразности столь длительного приема антикоагулянтов, если при чреспищеводной ЭхоКГ тромбоза предсердий не обнаружено (N. Engl. J. Med. 1993; 328:750).
в. Плановая кардиоверсия проводится в условиях стационара. Чем длительнее пароксизм, тем ниже вероятность восстановления синусового ритма. Насколько существенны размеры левого предсердия, неясно: некоторые считают, что шансы на успех кардиоверсии снижаются уже при переднезаднем размере, равном 45—50 мм.
1) Для медикаментозной кардиоверсии наиболее эффективны препараты классов Ia и Ic. Если с помощью препаратов класса Ia синусовый ритм восстановить не удалось, то в половине случаев это удается сделать с помощью пропафенона, соталола или амиодарона (J. Am. Coll. Cardiol. 1990; 15:698). Вероятность успеха:
а) длительность пароксизма б) длительность пароксизма > 2 сут: средства всех групп эффективны в 20—30% случаев.
2) Электрическая кардиоверсия. Начинают с разряда 100 Дж, энергия второго разряда — 200 Дж, третьего — 360 Дж. К электрической кардиоверсии обычно прибегают лишь после безуспешных попыток медикаментозного восстановления ритма. В то же время, если устранена причина мерцательной аритмии (гипокалиемия, тиреотоксикоз, ТЭЛА, перикардит и т. п.), можно сразу начать с электрической кардиоверсии. Если разрядами 100—200—360 Дж синусовый ритм восстановить не удалось, вводят прокаинамид, 500—750 мг в/в (скорость инфузии — не выше 30—50 мг/мин), затем повторяют разряд 360 Дж. При неэффективности перечисленных мер прибегают к внутрисердечной кардиоверсии (Circulation 1992; 86:1415).
4. После восстановления синусового ритма: продолжать прием препаратов классов Ia или Ic, блокаторов АВ-проведения и варфарина. Через 3 нед после восстановления ритма варфарин отменяют. Считается, что за это время сократимость предсердия полностью восстанавливается. Даже несмотря на постоянный прием средств классов Ia, Ic или амиодарона, лишь у 50% больных сохраняется синусовый ритм через год после успешной кардиоверсии.
5. Если синусовый ритм восстановить не удалось. Варианты лечения:
а. постоянный прием блокаторов АВ-проведения. Назначают дилтиазем, верапамил или бета-адреноблокаторы (в виде монотерапии) либо дилтиазем в сочетании с дигоксином. Эти средства позволяют добиться более устойчивого снижения ЧСС, чем монотерапия дигоксином (особенно при нагрузке);
б. деструкция пучка Гиса, затем — постоянная ЭКС в режиме VVIR;
в. операции на миокарде предсердий (в практику еще не внедрены).
6. Предупреждение пароксизмов
а. Первый пароксизм мерцательной аритмии. Если устранена причина аритмии, если пароксизм не сопровождался сердечной недостаточностью, стенокардией, артериальной гипотонией и ЧСС во время пароксизма была не слишком высокой, то профилактического лечения не требуется. В остальных случаях назначают блокаторы АВ-проведения и препараты класса Ia либо проводят монотерапию препаратом класса Ic.
б. Мерцательная аритмия в анамнезе. Если пароксизмы возникают редко и синусовый ритм восстанавливается самостоятельно, то постоянного лечения не требуется. Если же пароксизмы сопровождаются нарушениями гемодинамики или протекают с очень высокой ЧСС, то назначают блокаторы АВ-проведения.
в. Пароксизмы возникают часто либо вызывают тяжелые нарушения гемодинамики. Назначают блокаторы АВ-проведения, препараты классов Ia или Ic и варфарин (поддерживать МНО на уровне 2,0—3,0, а у больных с протезированными клапанами — на уровне 3,0—4,5). Больным моложе 60 лет с идиопатической мерцательной аритмией (без органического поражения сердца и артериальной гипертонии) в качестве первичной профилактики тромбоэмболий достаточно назначить аспирин (испытание SPAF, см. гл. 19, п. VIII.А.4).
Профилактика [ править ]
Прочее [ править ]
Любую тахикардию с узкими комплексами QRS и ЧСС около 150 уд/мин поначалу рассматривают как трепетание предсердий. Массаж каротидного синуса ведет к постепенному угнетению АВ-проведения; на этом фоне становятся видны волны трепетания предсердий. При синусовой тахикардии этот прием на короткое время снижает ЧСС, а при реципрокной наджелудочковой тахикардии он либо приводит к восстановлению синусового ритма, либо не вызывает изменений. Независимо от способа восстановления синусового ритма (электрическая или медикаментозная кардиоверсия, сверхчастая ЭКС) антикоагулянты не назначают. Снизить ЧСС обычно не удается, поэтому от медикаментозного лечения быстро переходят к кардиоверсии. Если предсердные импульсы проводятся на желудочки реже чем 2:1, то это может свидетельствовать о синдроме слабости синусового узла (см. гл. 6, п. IX). В подобных случаях после успешной кардиоверсии может развиться синоатриальная или АВ-блокада высокой степени; перед кардиоверсией таким больным устанавливают зонд-электрод для временной эндокардиальной ЭКС. ЭКГ — см. гл. 5, п. II.Б.3.
1. Восстановление синусового ритма:
а. кардиоверсия разрядом 50 Дж, затем (если аритмия сохраняется) — 100, 200, 360 Дж;
б. сверхчастая предсердная ЭКС, особенно если кардиоверсия противопоказана (из-за гликозидной интоксикации);
в. медикаментозное лечение само по себе восстанавливает синусовый ритм редко. Для повышения эффективности кардиоверсии и сверхчастой предсердной ЭКС, а также для поддержания синусового ритма, назначают блокаторы АВ-проведения (дигоксин, бета-адреноблокаторы, верапамил, дилтиазем) в сочетании с препаратами классов Ia, Ic или III. По мере снижения частоты предсердий АВ-проведение может улучшиться: необходимо следить за тем, чтобы не увеличилась частота желудочковых сокращений (из-за АВ-проведения 1:1).
2. Предупреждение пароксизмов:
а. препараты классов Ia, Ic или III;
б. при неэффективности медикаментозной профилактики — имплантация устройств для сверхчастой ЭКС, катетерная деструкция проводящих путей в предсердиях или разрушение АВ-узла с последующей постоянной желудочковой ЭКС;
в. оперативное лечение находится в стадии изучения.
Источники (ссылки) [ править ]
Что такое мерцательная аритмия (фибрилляция предсердий)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Меркушин Д. Е., онколога со стажем в 11 лет.
Определение болезни. Причины заболевания
Мерцательная аритмия (фибрилляция предсердий) — нарушение ритма работы сердца, при котором отсутствует механическая систола предсердий и имеет место хаотичная электрическая активность их миокарда, состояние сопровождается нерегулярными сокращениями желудочков и гемодинамическими расстройствами.
Признаки фибрилляции предсердий на ЭКГ:
Распространенность фибрилляции предсердий в общей популяции населения составляет от 1 до 2%.
В большинстве случаев развитие фибрилляции ассоциировано с органической патологией органов сердечно-сосудистой системы, создающих субстрат для сохранения фибрилляции, однако появление данного симптомокомплекса не всегда укладывается в какую-либо нозологическую категорию, в такой ситуации говорят об изолированной фибрилляции предсердий.
Строение и физиология сердца:
Заболевания, способствующие возникновению мерцательной аритмии
Среди ассоциированных с данной патологией заболеваний выделяют:
Факторы образа жизни, способствующие возникновению мерцательной аритмии
Чем опасна фибрилляция предсердий
Нарушение может приводить к развитию хронической сердечной недостаточности. Непоследовательное сокращение камер сердца способно значимо влиять на гемодинамику. Отсутствие скоординированного сокращения предсердий может снижать сердечный выброс примерно на 10 %. Такое снижение обычно хорошо переносится, кроме случаев с повышением частоты сокращений желудочков, когда ритм становится слишком частым (например, более 140 ударов/минуту) или когда у пациентов исходно имеется пограничный или сниженный сердечный выброс. В таких случаях может развиться сердечная недостаточность.
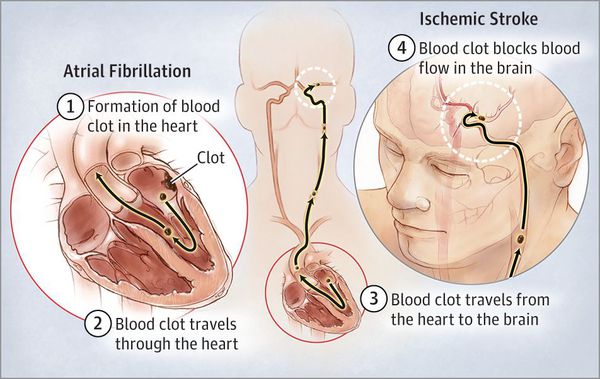
Развитие острого нарушения мозгового кровообращения. Риск развития ишемического инсульта составляет 1,5 % у лиц 50—59 лет и 23,5 % у лиц 80—89 лет. Особенно опасной является пароксизмальная фибрилляция предсердий с частыми срывами синусового ритма. Риск развития тромбоза церебральных сосудов особенно увеличивается в период срыва и восстановления синусового ритма. Выделяют т. н. атеротромботический подтип острого нарушения мозгового кровообращения по ишемическому типу.
Симптомы мерцательной аритмии
При фибрилляции предсердий отсутствует их эффективная механическая систола. При этом желудочки наполняются преимущественно пассивно за счет градиента давления между полостями сердца в период диастолы. В условиях увеличенной частоты сердечных сокращений не происходит достаточного наполнения желудочков, что приводит к гемодинамическим расстройствам различной степени выраженности.
Пациенты предъявляют жалобы на сердцебиение, чувство перебоя в ритме работы сердца, снижение работоспособности, повышенную утомляемость, одышку и сердцебиение при привычной ранее нагрузке. Кроме того, могут усугубляться симптомы уже существующих заболеваний сердечно-сосудистой системы.
Патогенез мерцательной аритмии
Хронические заболевания сердечно-сосудистой системы, а также состояния, характеризующиеся повышенной активностью РААС, вызывают структурное ремоделирование стенок предсердий и желудочков —пролиферацию и дифференцировку фибробластов в миофибробласты, синтез волокон соединительной ткани и развитие фиброза. Процессы ремоделирования камер сердца приводят к неоднородности проведения потенциала действия и к диссоциации сокращения мышечных пучков. При этом нарушается механическая систола предсердий и создаются условия для персистенции этого патологического состояния. [1]
Желудочки производят ненеритмичные сокращения, в итоге кровь задерживается в предсердиях, их объем увеличивается. Уменьшение наполнения желудочков, их частое сокращение, а также отсутствие эффективного сокращения предсердий могут приводить к снижению сердечного выброса и выраженным гемодинамическим расстройствам.
Из-за того, что кровоток в предсердиях замедляется из-за нарушения их механической систолы, а также из-за турбулентного перемешивания крови образуются тромбы, преимущественно в ушке левого предсердия.
Классификация и стадии развития мерцательной аритмии
Клинически различают несколько форм мерцательной аритмии, в зависимости от которых определяется тактика ведения пациента:
| Форма мерцательной аритмии | Описание |
|---|---|
| Впервые выявленная фибрилляцию предсердий | любой впервые возникший эпизод фибрилляции независимо от его причин и длительности |
| Пароксизмальная форма | периодические эпизоды фибрилляции предсердий длительностью до 7 суток с самопроизвольным прекращением |
| Персистирующая форма | эпизоды продолжительностью более 7 суток без самопроизвольного прекращения |
| Длительно персистирующая форма | эпизоды фибрилляции предсердий длятся более 1 года |
| Постоянная форма | присутствует постоянно |
В зависимости от присутствия искусственного клапана и поражений клапанного аппарата выделяют клапанную и неклапанную форму мерцательной аритмии.
Осложнения мерцательной аритмии
Чем опасна фибрилляция предсердий:
Таким образом, наблюдается тесная связь мерцательной аритмией с инсультом и сердечной недостаточностью.
Диагностика мерцательной аритмии
Обязательный минимум диагностики включает:
Могут применяться дополнительные методы обследования:
Лечение мерцательной аритмии
Экстренная помощь пациентам с острым приступом мерцательной аритмии
При впервые возникшем эпизоде фибрилляции предсердций каждому пациенту показана госпитализация в стационар круглосуточного пребывания. Госпитализация также показана пациентам с длительностью приступа более 24 часов.
Некоторой части пациентов с нечастыми пароксизмами фибрилляции предсердий допустимо самостоятельно принимать от 450 до 600 мг. Пропафенона однократно (терапия “таблетка в кармане”). Стоит отметить, что такой подход допустим лишь в случае эффективности и безопасности, проверенной при госпитализации.
Как вести себя в случае эпизода нарушения ритма
При возникновении одышки, головокружения, потере сознания, давящей боли за грудиной на фоне приступа самому пациенту или сопровождающему обязательно необходимо вызвать бригаду неотложной помощи.
Целями лечения мерцательной аритмии является:
Профилактика рисков формирования тромбов
Первостепенной задачей терапии фибрилляции предсердий является профилактика тромбососудистых осложнений.
При наличии патологии со стороны венозной системы нижних конечностей пациент должен быть проконсультирован сосудистым хирургом.
Чтобы снизить готовность тромбов к тромбообразованию, применяются прямые и непрямые антикоагулянты.
Показания для антикоагулянтной терапии и выбор препарата определяются риском тромбоэмболии, который рассчитывают по шкале CHADS2. Если сумма баллов по шкале CHADS2 ≥ 2, то при отсутствии противопоказаний показана длительная терапия пероральными антикоагулянтами. Однако антикоагулянтная терапия опасна кровотечениями. Для оценки риска данного осложнения разработана шкала HAS-BLED. Сумма баллов ≥ 3 указывает на высокий риск кровотечения, и применение любого антитромботического препарата требует особой осторожности.
К антикоагулянтам непрямого действия относится антагонист витамина К варфарин. Препарат относится к группе антиметаболитов и нарушает синтез в печени X фактора свертывания.
К прямым антикоагулянтам относят гепарин и низкомолекулярные препараты гепарина (фраксипарин, эноксапарин и др.). Перевод пациентов с непрямого антикоагулянта на прямой рекомендован при необходимости хирургического лечения в связи с удобством коррекции терапевтического диапазона дозы.
К новым непрямым антикоагулянтам относят препараты прямые ингибиторы тромбина (дабигатран) и ингибиторы Xа фактора свертывания крови (препараты из группы ксабанов — апиксабан, ривароксабан, эдоксабан). Препараты обладают эффективностью, сопоставимой с приемом варфарина при минимуме гемморагических осложнений. Доказательная база у препаратов существует на данный момент только по проблеме неклапанной фибрилляции предсердий. Эффективность препаратов относительно клапанной фибрилляции предсердий в настоящее время является предметом клинических исследований. Поэтому при наличии врожденной и приобретенной патологии клапанного аппарата и наличии искусственного клапана сердца единственным препаратом из группы антикоагулянтов по-прежнему остается варфарин.
Восстанавливать или не восстанавливать синусовый ритм
Выбор стратегии ведения проводится индивидуально. Учитывается возраст пациента, выраженность симптомов фибрилляции предсердий, наличие структурной патологии миокарда, физическая активность.
Удержание стабильного сердечного ритма
Длительная терапия фибрилляции предсердий предполагает выбор стратегии — поддержания синусового ритма или контроля частоты сокращений сердца.
При пароксизмальной фибрилляции возможно рассмотреть тактику поддержания синусового ритма.
При персистирующей и постоянной форме, пожилом возрасте, низкой физической активности и удовлетворительной субъективной переносимости фибрилляции большинство специалистов склоняются к тактике контроля ЧСС, т. к. восстановление синусового ритма и его последующий срыв сопровождаются изменениями реологических свойств крови и повышенным риском внутрисосудистого тромбообразования, а тактика поддержания синусового ритма не улучшает отдаленный прогноз у пациентов.
Контроль ЧСС
Стратегия контроля частоты сердечных сокращений предполагает регулярный прием частотоурежающих препаратов из группы сердечных гликозидов, бета-адреноблокаторов, блокаторов Са++ каналов и антиаритмиков III класса (амиодарон, дронедарон), а также используются их комбинации.
При подборе препаратов важно знать, есть ли у пациента трепетание предсердий. Это нарушение часто сочетается с фибрилляцией. Если доктор не учтёт это сочетание при подборе терапии, препараты будут воздействовать только на фибрилляцию, а трепетание сохранится. Это чревато развитием сердечной недостаточности: трепетание приводит к нему быстрее, чем фибрилляция.
Сегодня не существует точного ответа на вопрос о целевом уровне ЧСС при фибрилляции предсердий. Клинические и методические рекомендации основаны на мнении экспертов в области кардиологии.
Первоначально рекомендуется снизить частоту сокращения желудочков до уровня менее 110 ударов в покое и при физической нагрузке. Если урежение частоты сокращения желудочков не приводит к исчезновению ограничений физической активности, то целесообразно снизить частоту их сокращений до 60-80 в покое и 90-115 в минуту при физической нагрузке.
Из бета-адреноблокаторов применяются:
Среди недигидроперидиновых антагонистов Са++ назначают:
Из антиаритмиков III класса используют:
Имеются клинические данные об эффективности омега-3 полиненасыщенных жирных кислот в комплексной терапии фибрилляции предсердий, в частности эйкозапентаеновой и докозагексаеновой. По данным многоцентровых плацебо-контролируемых клинических исследований FORWARD и OPERA, доказано влияние омега-3 полиненасыщенных жирных кислот на снижение риска внезапной смерти и общую летальность пациентов, имеющих хроническую сердечную недостаточность, и пациентов, перенесших острый инфаркт миокарда. [3]
По данным исследования GISSI-Prevenzione, назначение омега-3 полиненасыщенных жирных кислот позволяет снизить рецидивы фибрилляции предсердий уже через 3 недели от старта терапии. Максимальный эффект наблюдается через год непрерывного приема препарата. [4]
Стратегия контроля синусового ритма не исключает стратегию контроля частоты сердечных сокращений. Уменьшение частоты желудочковых сокращений до целевого уровня позволяет уменьшить клиническую симптоматику фибрилляции предсердий во время неизбежных срывов ритма работы предсердий.
Тактика контроля ритма не имеет существенного преимущества перед тактикой контроля частоты сокращений сердца в плане прогноза сердечно-сосудистой смертности, однако значительно уменьшает выраженность клинической симптоматики, возникающей при данном заболевании.
Препараты для восстановления синусового ритма
Для поддержания синусового ритма при фибрилляции предсердий рекомендуется применение следующих препаратов:
При развившемся пароксизме фибрилляции предсердий синусовый ритм восстанавливается спонтанно самостоятельно в течение нескольких часов или суток (до 7 суток).
При выраженной клинической симптоматике заболевания, а также если в дальнейшем будет выбрана стратегия поддержания синусового ритма, необходима медикаментозная кардиоверсия.
Для профилактики тромбососудистых осложнений пациенту предлагается прием 500 мг. ацетилсалициловой кислоты (кишечнорастворимую таблетку необходимо разжевать перед приемом) или 2 тб. (150 мг) клопидогрела.
Электрическая кардиоверсия
Электрическая кардиоверсия постоянным током быстро и эффективно переводит фибрилляцию предсердий в синусовый ритм. Предпочтение данному виду восстановления синусового ритма отдается при нестабильной гемодинамике (нарастающим симптомам хронической сердечной недостаточности) и появлению ишемии миокарда по ЭКГ/ЭХО-КС.
Радиочастотная катетерная абляция
Данные о выполнении радиочастотной абляции в терапии первой линии у пациентов с фибрилляцией предсердий остаются противоречивыми, в то время как у пациентов с рецидивирующей фибрилляцией эта процедура является максимально оправданной и эффективной.
Выявлены неблагоприятные факторы, увеличивающие частоту рецидивов после проведения данной процедуры : дилатация левого предсердия, возраст старше 65 лет, длительность заболевания, количество ранее проведенных процедур, а также недостаточность аортального и митрального клапанов.
Виды оперативного вмешательства при мерцательной аритмии
При мерцательной аритмии применяются хирургические методы лечения. Одним из вариантов является операция типа «лабиринта» Кокса. Суть операции заключается в изоляции задней стенки левого предсердия, каватрикуспидального и кавакавального перешейка и исключение из кровотока устья левого предсердия. Таким образом, операция создает электрический лабиринт ходов для распространения возбуждения, через которые импульс из синоатриального узла находит путь к предсердножелудочковому узлу, предотвращая формирование волн «re-entry». Операции типа “лабиринт” Кокса в основном использовались у пациентов, подвергающихся другим открытым операциям на сердце. Выполнение подобных сочетанных операций при мерцательной аритмии приводит к уменьшению рецидивов фибрилляции, трепетания предсердий и предсердных тахикардий, однако не влияет на общую смертность. Отбор пациентов на подобные методы хирургического лечения должен осуществляться на мультидисциплинарном консилиуме специалистов.
Хирургическая изоляция ушка левого предсердия выполнялась кардиоторакальными хирургами в течение нескольких десятилетий, однако проспективные рандомизированные исследования влиянии на частоту развития ишемического инсульта у пациентов после хирургического лечения в настоящее время отсутствуют.
Прогноз. Профилактика
Пароксизмальная и персистирующая формы фибрилляции предсердий могут оказаться, поводом для освобождения от труда с выдачей листка нетрудоспособности. Ориентировочный срок для освобождения от труда с целью купирования приступа — 7-10 дней; для подбора противорецидивной терапии требуется в среднем от 7 до 18 дней. [6] Критериями закрытия листка временной нетрудоспособности являются: