конец генетического кода диагноз
Эволюция генетического кода
Эволюция генетического кода
Рисунок с обложки журнала PNAS со статьей о механизме возникновения альтернативного генетического кода, объясняющей различия митохондриального генетического кода иглокожих перистых звезд и пчёл. Автор рисунка: Michael Plenikowski (University of Mainz, Mainz, Germany).
Автор
Редакторы
Генетический код — это «алфавит», лежащий в основе функционирования любой живой системы на Земле. Ранее считавшийся неизменным и универсальным для всех организмов, генетический код, на самом деле, подвержен эволюционному процессу, в результате которого могут возникать различные аномалии — например, варианты кода, специфичные для отдельных биологических видов или даже субклеточных органелл (митохондрий). Одна из таких аномалий, по-видимому, представляет собой древнюю адаптацию, защищающую от окислительного стресса, вызванного переходом к аэробному дыханию, и приводящую к высокой концентрации метионина в митохондриях.
Люди и многие другие животные используют два генетических кода для трансляции наследственной информации — стандартный код для белков, закодированных в клеточном ядре, и более «современный» вариант кода для трансляции митохондриального генома. Несмотря на первостепенное значение генетического кода в биологии, причины существования альтернативного кода в митохондриях оставались загадочными с момента его открытия в 1979 году. Различные гипотезы, касающиеся причин возникновения изменений в генетическом коде, отдавали предпочтение нейтральным эволюционным механизмам, поскольку принцип кодирования аминокислот не должен был меняться. Считалось, что любое изменение «смысла» отдельного кодона приведет к ошибкам в каждом транслируемом белке, что не может не иметь пагубных последствий для клетки. Адаптивное преимущество подобных изменений ставилось под сомнение. Согласно гипотезе «захвата кодона», GC-богатые кодоны могут исчезать из генома в результате изменения общего содержания нуклеотидных остатков G и C. (Известно, что геномы различных организмов могут существенно отличатся по этому параметру: сравните, например, АТ-богатый (75%) геном Micoplasma capricolum и GC-богатый (74%) геном Micrococcus luteus.) Как только кодон исчезает из генома организма, он теоретически может появиться снова в результате дрейфа генов. Такой кодон может быть «захвачен» путём неверного прочтения какой-нибудь тРНК из другой семьи кодонов. Таким образом, перекодировка кодона происходит абсолютно нейтрально и без появления «нездоровых» белков.
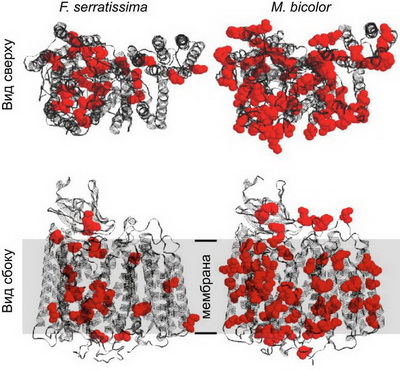
Рисунок 1. Структурные модели белков электронтранспортной цепи (комплекса цитохромоксидазы COX), кодируемых геномом митохондрий перистой морской звезды (иглокожее Florometra serratissima) и пчелы (Melipona bicolor). Вид сверху соответствует виду из митохондриального внутримембранного пространства, вид сбоку — те же структуры, внутримембранное пространство сверху. Остатки метионина отмечены красным.
Вопреки гипотезе «захвата кодона», гипотеза «двусмысленного прочтения» предлагает механизм, не являющийся нейтральным. Согласно этой гипотезе, мутации в тРНК приводят к тому, что считывание кодона осуществляется двумя различными тРНК — обычной и мутантной, — «заряженными» различными аминокислотами, но узнающими один и тот же кодон. Такая двусмысленность в прочтении кодона является критическим начальным этапом в процессе последовательного перекодирования кодона. Затем мутантная тРНК постепенно займёт место обычной, которая будет утеряна в результате случайных мутаций. Изменение GC-содержания не играет при таком сценарии определяющей роли, и весь процесс определяется полезностью изменений на уровне синтезируемых белков, другими словами — появлением или отсутствием адаптаций.
В статье, опубликованной группой исследователей из Университета Иоганна Гутенберга в Майнце, впервые показано, что причиной переопределения кодона AUA с кодирующего изолейцин на кодирующий метионин (что и наблюдается в митохондриях многих организмов) являются значительные и благоприятные в эволюционном плане изменения на уровне кодируемых белков.
Митохондрии — это «энергетические станции» клеток, перерабатывающие химическую энергию, выделяемую при окислении питательных веществ, и запасающие её в виде энергии ковалентных связей в молекуле аденозинтрифосфата (АТФ). Электрон-транспортная цепь, представляющая собой набор белков-ферментов, расположенных во внутренней мембране митохондрий, является ключевым узлом, производящим АТФ. Несмотря на то, что этот узел является жизненно важным, в качестве побочных продуктов он производит активные формы кислорода (сокращённо АФК), способные инициировать распространение свободных радикалов, повреждающих клетку, вызывающих болезни и, возможно, являющихся одной из причин старения. Поэтому митохондрии выработали различные механизмы защиты, препятствующие появлению АФК и распространению свободных радикалов.
Авторы статьи убедительно продемонстрировали, что переопределение кодона (с изолейцина на метионин) в митохондриях организмов, активно использующих аэробное дыхание (например, пчёл, но не «мало дышащих» иглокожих), привело к значительному накоплению легко окисляемых аминокислотных остатков метионина в белках, находящихся в богатой окислителями внутренней мембране митохондрий. Этот видимый парадокс легко разрешается, если принять во внимание антиокислительные свойства метионина. В своей работе учёные представили экспериментальные доказательства того, что присутствие метионина в качестве антиоксиданта во внутренней мембране создаёт дополнительный барьер для разрушительного влияния АФК. Метионин является природным, отобранным в процессе эволюции, антиоксидантом, необходимым для функционирования электрон-транспортной цепи митохондрий и защищающий их от окислительного стресса.
Таким образом, коллективное изменение последовательностей белков в результате переопределения кодона может предоставлять преимущество в процессе естественного отбора, что подтверждает гипотезу «двусмысленного кодирования», объясняющую эволюцию генетического кода. Другими словами, окислительный стресс сформировал митохондриальный генетический код.
32. Клетка как биологическая система  Читать 0 мин.
Читать 0 мин.
32.275. Генетический код и его свойства
Ранее мы подчёркивали, что нуклеотиды имеют важную для формирования жизни на Земле особенность ― при наличии в растворе одной полинуклеотидной цепочки спонтанно происходит процесс образования второй (параллельной) цепочки на основании комплементарного соединения родственных нуклеотидов. Одинаковое число нуклеотидов, в обоих цепочках и их химическое родство, является непременным условием для осуществления такого рода реакций. Однако при синтезе белка, когда информация с иРНК реализуется в структуру белка никакой речи о соблюдении принципа комплементарности идти не может. Это связано с тем, что в иРНК, и в синтезированном белке различно не только число мономеров, но и, что особенно важно, отсутствует структурное сходство между ними (с одной стороны нуклеотиды, с другой аминокислоты). Понятно, что в этом случае возникает необходимость создания нового принципа точного перевода информации с полинуклеотида в структуру полипептида. В эволюции такой принцип был создан и в его основу был заложен генетический код.
Генетический код ― это система записи наследственной информации в молекулах нуклеиновых кислот, основанная на определённом чередовании последовательностей нуклеотидов в ДНК или РНК, образующих кодоны, соответствующие аминокислотам в белке.
Генетический код имеет несколько свойств:
Следует отметить, что некоторые авторы предлагают ещё и другие свойства кода, связанные с химическими особенностями входящих в код нуклеотидов или с частотой встречаемости отдельных аминокислот в белках организма и т.д. Однако эти свойство вытекают из вышеперечисленных, поэтому там мы их и рассмотрим.
Генетический код, как и многое сложно организованные система имеет наименьшую структурную и наименьшую функциональную единицу. Триплет ― наименьшая структурная единица генетического кода. Состоит она из трёх нуклеотидов. Кодон ― наименьшая функциональная единица генетического кода. Как правило, кодонами называют триплеты иРНК. В генетическом коде кодон выполняет несколько функций. Во-первых, главная его функция заключается в том, что он кодирует одну аминокислоту. Во-вторых, кодон может не кодировать аминокислоту, но, в этом случае, он выполняет другую функцию (см. далее). Как видно из определения, триплет ― это понятие, которое характеризует элементарную структурную единицу генетического кода (три нуклеотидов). Кодон ― характеризует элементарную смысловую единицу генома ― три нуклеотида определяют присоединение к полипептидной цепочки одной аминокислоты.
Элементарную структурную единицу вначале расшифровали теоретически, а затем её существование подтвердили экспериментально. И действительно, 20 аминокислот невозможно закодировать одним или двумя нуклеотидом т.к. последних всего 4. Три нуклеотида из четырёх дают 43 = 64 варианта, что с избытком перекрывает число имеющихся у живых организмах аминокислот (см.табл. 1).
Представленные в таблице 64 сочетания нуклеотидов имеют две особенности. Во-первых, из 64 вариантов триплетов только 61 являются кодонами и кодируют какую-либо аминокислоту, их называют смысловые кодоны. Три триплета не кодируют.
Таблица 1.
Кодоны информационной РНК и соответствующие им аминокислотыявляются стоп-сигналами, обозначающие конец трансляции. Таких триплетов три ― УАА, УАГ, УГА, их ещё называют «бессмысленные» (нонсенс кодоны). В результате мутации, которая связана с заменой в триплете одного нуклеотида на другой, из смыслового кодона может возникнуть бессмысленный кодон. Такой тип мутации называют нонсенс-мутация. Если такой стоп-сигнал сформировался внутри гена (в его информационной части), то при синтезе белка в этом месте процесс будет постоянно прерываться ― синтезироваться будет только первая (до стоп-сигнала) часть белка. У человека с такой патологией будет ощущаться нехватка белка и возникнут симптомы, связанные с этой нехваткой. Например, такого рода мутация выявлена в гене, кодирующем бета-цепь гемоглобина. Синтезируется укороченная неактивная цепь гемоглобина, которая быстро разрушается. В результате формируется молекула гемоглобина, лишённая бета-цепи. Понятно, что такая молекула вряд ли будет полноценно выполнять свои обязанности. Возникает тяжёлое заболевания, развивающееся по типу гемолитической анемии (бета-ноль талассемия, от греческого слова «Таласа» ― Средиземное море, где эта болезнь впервые обнаружена).
Механизм действия стоп-кодонов отличается от механизма действия смысловых кодонов. Это следует из того, что для всех кодоны, кодирующие аминокислоты, найдены соответствующие тРНК. Для нонсенс-кодонов тРНК не найдены. Следовательно, в процессе остановки синтеза белка тРНК не принимает участие.
Кодон АУГ (у бактерий иногда ГУГ) не только кодируют аминокислоту метионин и валин, но и является инициатором трансляции.
61 из 64 триплетов кодируют 20 аминокислот. Такое трёхразовое превышение числа триплетов над количеством аминокислот позволяет предположить, что в переносе информации могут быть использованы два варианта кодирования. Во-первых, не все 64 кодона могут быть задействованы в кодировании 20 аминокислот, а только 20 и, во-вторых, аминокислоты могут кодироваться несколькими кодонами. Исследования показали, что природа использовала последний вариант.
Код, при котором одна аминокислота кодируется несколькими триплетами, называется вырожденным или избыточным. Почти каждой аминокислоте соответствует несколько кодонов. Так, аминокислота лейцин может кодироваться шестью триплетами — УУА, УУГ, ЦУУ, ЦУЦ, ЦУА, ЦУГ. Валин кодируется четырьмя триплетами, фенилаланин — двумя и только триптофан и метионин кодируются одним кодоном. Свойство, которое связано с записью одной и той же информации разными символами носит название вырожденность.
Число кодонов, предназначенных для одной аминокислоты, хорошо коррелируется с частотой встречаемости аминокислоты в белках. И это, скорее всего, не случайно. Чем больше частота встречаемости аминокислоты в белке, тем чаще представлен кодон этой аминокислоты в геноме, тем выше вероятность его повреждения мутагенными факторами. Поэтому понятно, что мутированный кодон имеет больше шансов кодировать туже аминокислоту при высокой его вырожденности. С этих позиций вырожденность генетического кода является механизмом защищающим геном человека от повреждений.
Необходимо отметить, что термин вырожденность используется в молекулярной генетики и в другом смысле. Так основная часть информации в кодоне приходится на первые два нуклеотида, основание в третьем положении кодона оказывается малосущественным. Этот феномен называют “вырожденностью третьего основания”. Последняя особенность сводит до минимума эффект мутаций. Например, известно, что основной функцией эритроцитов крови является перенос кислорода от легких к тканям и углекислого газа от тканей к легким. Осуществляет эту функцию дыхательный пигмент — гемоглобин, который заполняет всю цитоплазму эритроцита. Состоит он из белковой части ― глобина, который кодируется соответствующим геном. Кроме белка в молекулу гемоглобина входит ген, содержащий железо. Мутации в глобиновых генах приводят к появлению различных вариантов гемоглобинов. Чаще всего мутации связаны с заменой одного нуклеотида на другой и появлением в гене нового кодона, который может кодировать новую аминокислоту в полипептидной цепи гемоглобина. В триплете, в результате мутации может быть заменён любой нуклеотид ― первый, второй или третий.
Известно несколько сотен мутаций, затрагивающих целостность генов глобина. Около 400 из них связаны с заменой единичных нуклеотидов в гене и соответствующей аминокислотной заменой в полипептиде. Из них только 100 замен приводят к нестабильности гемоглобина и различного рода заболеваниям от легких до очень тяжелых. 300 (примерно 64%) мутаций-замен не влияют на функцию гемоглобина и не приводят к патологии. Одной из причин этого является упомянутая выше “вырожденность третьего основания”, когда замена третьего нуклеотида в триплете, кодирующем серин, лейцин, пролин, аргинин и некоторые другие аминокислоты приводит к появлению кодона-синонима, кодирующего ту же аминокислоту. Фенотипически такая мутация не проявится. В отличие от этого любая замена первого или второго нуклеотида в триплете в 100 % случаях приводит к появлению нового варианта гемоглобина. Но и в этом случае тяжёлых фенотипических нарушений может и не быть. Причиной этому является замена аминокислоты в гемоглобине на другую сходную с первой по физико-химическим свойствам. Например, если аминокислота, обладающая гидрофильными свойствами, заменена на другую аминокислоту, но с такими же свойствами.
Гемоглобин состоит из железопорфириновой группы гема (к ней и присоединяются молекулы кислорода и углекислоты) и белка — глобина. Гемоглобин взрослого человека (НвА) содержит две идентичные a-цепи и две b-цепи. Замена в гене, кодирующем b-цепь гемоглобина первого или второго нуклеотида практически всегда приводит к появлению в белка новых аминокислот, нарушению функций гемоглобина и тяжёлым последствия для больного. Например, замена “Ц” в одном из триплетов ЦАУ (гистидин) на “У” — приведет к появлению нового триплета УАУ, кодирующего другую аминокислоту — тирозин. Фенотипически это проявится в тяжёлом заболевании. Аналогичная замена в 63 положении b-цепи полипептида гистидина на тирозин приведет к дестабилизации гемоглобина. Развивается заболевание метгемоглобинемия. Замена, в результате мутации, глутаминовой кислоты на валин в 6-м положении b-цепи является причиной тяжелейшего заболевания — серповидно-клеточной анемии. Не будем продолжать печальный список. Отметим только, что при замене первых двух нуклеотидов может появится аминокислота по физико-химическим свойствам похожая на прежнюю. Так, замена 2-го нуклеотида в одном из триплетов, кодирующего глутаминовую кислоту (ГАА) в b-цепи на “У” приводит к появлению нового триплета (ГУА), кодирующего валин, а замена первого нуклеотида на “А” формирует триплет ААА, кодирующий аминокислоту лизин. Глутаминовая кислота и лизин сходны по физико-химическим свойствам — они обе гидрофильны. Валин — гидрофобная аминокислота. Поэтому, замена гидрофильной глютаминовой кислоты на гидрофобный валин, значительно меняет свойства гемоглобина, что, в конечном итоге, приводит к развитию серповидноклеточной анемии, замена же гидрофильной глютаминовой кислоты на гидрофильный лизин в меньшей степени меняет функцию гемоглобина — у больных возникает легкая форма малокровия. В результате замены третьего основания новый триплет может кодировать туже аминокислоты, что и прежней. Например, если в триплете ЦАУ урацил был заменён на цитозин и возник триплет ЦАЦ, то практически никаких фенотипических изменений у человека выявлено не будет. Это понятно, т.к. оба триплета кодируют одну и туже аминокислоту ― гистидин.
В заключении уместно подчеркнуть, что вырожденность генетического кода и вырожденность третьего основания с общебиологических позиция являются защитными механизмами, которые заложены в эволюции в уникальной структуре ДНК и РНК.
Каждый триплет (кроме бессмысленных) кодирует только одну аминокислоту. Таким образом, в направлении кодон ― аминокислота генетический код однозначен, в направлении аминокислота ― кодон ― неоднозначен (вырожденный).
И в этом случае необходимость однозначности в генетическом коде очевидна. При другом варианте при трансляции одного и того же кодона в белковую цепочку встраивались бы разные аминокислоты и в итоге формировались белков с различной первичной структурой и разной функцией. Метаболизм клетки перешёл бы в режим работы «один ген ― несколько поипептидов». Понятно, что в такой ситуации регулирующая функция генов была бы полностью утрачена.
Считывание информации с ДНК и с иРНК происходит только в одном направлении. Полярность имеет важное значение для определения структур высшего порядка (вторичной, третичной и т.д.). Ранее мы говорили о том, что структуры низшего порядка определяют структуры более высшего порядка. Третичная структура и структуры более высокого порядка у белков, формируются сразу же как только синтезированная цепочка РНК отходит от молекулы ДНК или цепочка полипептида отходит от рибосомы. В то время, когда свободный конец РНК или полипептида приобретает третичную структуру, другой конец цепочки ещё продолжает синтезироваться на ДНК (если транскрибируется РНК) или рибосоме (если транскрибируется полипептид).
Поэтому однонаправленный процесс считывания информации (при синтезе РНК и белка) имеет существенное значение не только для определения последовательности нуклеотидов или аминокислот в синтезируемом веществе, но для жёсткой детерминации вторичной, третичной и т.д. структур.
Код может быть перекрывающимся и не перекрывающимся. У большинства организмов код не перекрывающийся. Перекрывающийся код найден у некоторых фагов.
Сущность не перекрывающего кода заключается в том, что нуклеотид одного кодона не может быть одновременно нуклеотидом другого кодона. Если бы код был перекрывающим, то последовательность из семи нуклеотидов (ГЦУГЦУГ) могла кодировать не две аминокислоты (аланин-аланин) (рис.33, А) как в случае с не перекрывающимся кодом, а три (если общим является один нуклеотид) (рис. 33, Б) или пять (если общими являются два нуклеотида) (см. рис. 33, В). В последних двух случаях мутация любого нуклеотида привела бы к нарушению в последовательности двух, трёх и т.д. аминокислот.
Однако установлено, что мутация одного нуклеотида всегда нарушает включение в полипептид одной аминокислоты. Это существенный довод в пользу того, что код является не перекрывающимся. Неперекрываемость генетического кода связана с ещё одним свойством ― считывание информации начинается с определённой точки ― сигнала инициации. Таким сигналом инициации в иРНК является кодон, кодирующий метионин АУГ. Следует отметить, что у человека всё-таки имеется небольшое число генов, которые отступают от общего правила и перекрываются.
Между кодонами нет знаков препинания. Иными словами триплеты не отделены друг от друга, например, одним ничего не значащим нуклеотидом. Отсутствие в генетической коде «знаков препинания» было доказано в экспериментах.
Код един для всех организмов, живущих на Земле. Прямое доказательство универсальности генетического кода было получено при сравнении последовательностей ДНК с соответствующими белковыми последовательностями. Оказалось, что во всех бактериальных и эукариотических геномах используется одни и те же наборы кодовых значений. Есть и исключения, но их не много.
Первые исключения из универсальности генетического кода были обнаружены в митохондриях некоторых видов животных. Это касалось кодона терминатора УГА, который читался так же как кодон УГГ, кодирующий аминокислоту триптофан. Были найдены и другие более редкие отклонения от универсальности.
Для повторения:
Генетический код ― это система записи наследственной информации в молекулах нуклеиновых кислот, основанная на определённом чередовании последовательностей нуклеотидов в ДНК или РНК, образующих кодоны, соответствующие аминокислотам в белке. Генетический код имеет несколько свойств.
1. Триплетность. Триплет состоит из трёх нуклеотидов. 61 кодон ― смысловые, т.е. кодируют какую-либо аминокислоту, три ― бессмысленные, т.е. не кодируют аминокислоты.
2. Вырожденность или избыточность. Одна аминокислота может кодироваться несколькими кодонами.
3. Однозначность. Один кодон кодирует только одну аминокислоту.
4. Полярность. Считывание информации с ДНК и с иРНК происходит только в одном направлении.
5. Неперекрываемость. Генетический код является не перекрывающимся.
6. Компактность. Между кодонами нет знаков препинания.
7. Универсальность. Код един для всех живущих на земле организмов.
Причины генетического бесплодия
Согласно оценкам экспертов Всемирной организации здравоохранения, около 50 миллионов супружеских пар во всем мире (что составляет примерно 7% от их общего количества) не могут завести ребенка из-за мужского и/или женского бесплодия. На данный момент считается, что в 50% случаев причиной являются генетические нарушения.
Современная наука достигла больших успехов в изучении причин генетического бесплодия, особенно с появлением метода секвенирования нового поколения (next generation sequencing, NGS), позволяющего быстро и с минимальными трудозатратами «читать» последовательность ДНК. Тем не менее, этот вопрос остается сложным, и в имеющихся на данный момент знаниях остается еще немало пробелов.
Существует множество генов, влияющих на мужскую и женскую репродуктивную функцию. Например, в одних только яичках мужчины экспрессируется около 2300 генов. Наука продолжает развиваться, и список доступных анализов ежегодно пополняется новыми генетическими тестами.
Генетические изменения, способные приводить к невозможности зачатия и вынашивания беременности, бывают разными:
Хромосомные аномалии
Хромосомные нарушения представляют большой интерес в аспекте вопросов бесплодия, так как они ответственны более чем за половину всех выкидышей в первом триместре беременности. В большинстве случаев хромосомные аномалии не наследуются – они возникают случайно в половых клетках или клетках эмбриона. При этом происходят выкидыш, мертворождение, либо ребенок рождается с серьезными пороками развития.
В каждой клетке человеческого тела содержится 46 хромосом. В яйцеклетке и сперматозоиде их по 23 – соответственно, ребенок получает половину набора от матери и половину от отца. Состояние, при котором меняется количество хромосом, называется анеуплоидией. Некоторые примеры, связанные с бесплодием:
Помимо изменений количества хромосом, встречаются нарушения их структуры – аберрации.
Их основные разновидности:
Моногенные заболевания
Моногенные заболевания характеризуются возникновением мутации в одном гене, отвечающем за синтез определенного белка. Эти патологии передаются от родителей детям, причем типы наследования бывают разными.
В настоящее время известно много моногенных мутаций, связанных с бесплодием. Их список постоянно пополняется.
Мультифакториальные заболевания
Мультифакториальные, или полигенные заболевания имеют сложный патогенез. В их развитии принимают участие генетические нарушения (как наследственные, так и приобретенные), образ жизни, воздействия внешней среды. На «неправильные» гены накладываются такие факторы, как особенности питания, уровень физической активности, экологическая обстановка, вредные привычки, стрессы, прием различных лекарственных препаратов и пр.
Типичные примеры мультифакториальных заболеваний – сахарный диабет и сердечно-сосудистые патологии. Среди причин женского бесплодия важное значение имеют следующие заболевания:
Эпигенетические изменения
Эпигенетические изменения возникают в результате различных процессов, когда последовательность ДНК остается нормальной, но меняется активность генов. Например, это происходит в результате метилирования – прикрепления особых метильных групп к определенным участкам ДНК. Некоторые научные исследования показали, что эпигенетические механизмы играют роль в развитии бесплодия.
В каких случаях рекомендуется пройти генетическое тестирование?
Обычно врачи направляют пациентов на консультации к клиническим генетикам в следующих случаях:
Генетик собирает семейный анамнез, анализирует родословную и при необходимости назначает анализы. Для диагностики причин генетического бесплодия применяют разные методы: цитогенетический анализ, полимеразную цепную реакцию (ПЦР), флуоресцентную гибридизацию in situ (FISH), микрочипирование, секвенирование нового поколения.
Чтобы выявить распространенные аномалии у плода, на 16–20-й неделях беременности проводят тройной тест. По показаниям выполняют различные инвазивные исследования. Более современный и точный метод диагностики – неинвазивное пренатальное тестирование (НИПТ), во время которого изучают ДНК плода в крови матери.
Если у одного или обоих партнеров из пары, страдающей бесплодием, выявляют генетические нарушения, в ряде случаев могут помочь различные методы лечения или вспомогательные репродуктивные технологии (ЭКО, ИКСИ). Но иногда проблему не удается решить. В таких ситуациях врач предложит рассмотреть возможность использования донорских яйцеклеток или сперматозоидов.
С возрастом репродуктивные возможности уменьшаются, а в клетках накапливаются мутации, которые могут помешать наступлению и вынашиванию беременности, вызвать тяжелые патологии у ребенка. Поэтому женщинам, которые планируют забеременеть после 35 лет, стоит подумать о возможности сохранить свои яйцеклетки в криобанке. В дальнейшем ими можно воспользоваться в любое время – это будет своего рода «страховка» репродуктивной функции.
Если вы решили сохранить собственные половые клетки или воспользоваться донорскими, важно подобрать надежный банк половых клеток. На данный момент Репробанк является одним из крупнейших на территории России и СНГ. Наше криохранилище оснащено новейшим оборудованием, а в каталоге представлено большое количество доноров, среди которых любая пара наверняка сможет подобрать подходящего.
Зиновьева Юлия Михайловна
Ведёт генетическое обследование доноров Репробанка, осуществляет подбор доноров для пар, имеющих ранее рождённых детей с установленной генетической патологией.
 Читать 0 мин.
Читать 0 мин.