мегалобластическая анемия что это
Мегалобластная анемия
Мегалобластные анемии являются результатом дефицита витамина В12 и фолиевой кислоты. Неэффективный гемопоэз поражает все клеточные линии, но в особенности эритроидную. Диагноз базируется на общем анализе крови, мазке периферической крови, в которых определяется макроцитарная анемия с анизоцитозом и пойкилоцитозом, большие овальные эритроциты (макроовалоциты), гиперсегментация нейтрофилов и ретикулоцитопения. Лечение направлено на устранение основной причины.
Причины мегалобластных анемий
Наиболее частой причиной межобластного кроветворения является нарушение утилизации витамина В12 или фолиевой кислоты. Другими причинами являются употребление лекарственных препаратов (обычно цитостатических или иммунодепрессантов), нарушающих синтез ДНК, и реже метаболические заболевания. В некоторых случаях этиология мегалобластоза неизвестна.
Патофизиология мегалобластных анемий
Мегалобластный тип кроветворения является результатом нарушения синтеза ДНК, приводя к появлению больших клеток с крупными ядрами. Во всех клеточных линиях имеет место нарушение созревания, при котором созревание цитоплазмы опережает созревание ядер, это приводит к появлению мегалобластов в костном мозге, прежде чем происходят изменения в крови. Нарушение гемопоэза вызывает костномозговую гибель клеток, делая эритропоэз неэффективным, и непрямую гипербилирубинемию и гиперурикемию. Поскольку нарушение созревания поражает все клеточные линии, определяется ретикулоцитопения, в более поздних стадиях лейкопения и тромбоцитопения. Большие овальные эритроциты (макроовалоциты) появляются в кровотоке. Характерны гиперсегментированные полиморфноядерные нейтрофилы, механизм образования которых неясен.
Симптомы мегалобластных анемий
Большинство макроцитарных (MCV > 95 fl/клетку) анемий являются межобластными. Немегалобластный макроцитоз проявляется при различных клинических состояниях, не все из которых ясны. Анемия обычно развивается по механизмам, не зависящим от макро-цитоза. Макроцитоз, обусловленный избытком мембраны эритроцитов, проявляется у больных с хроническим заболеванием печени, при котором нарушается этерификация холестерина. Макроцитоз с MCV от 95 до 105 95А/клетку проявляется при хроническом алкоголизме с отсутствием дефицита фолие-вой кислоты. Умерено выраженный макроцитоз встречается при апластической анемии, особенно в период восстановления. Макроцитоз типичен и для миелоидисплазии. Вследствие того что эритроциты модифицируют свою форму в селезенке после выхода из костного мозга, макроцитоз может наблюдаться после спленэктомии, хотя эти изменения не ассоциированы с анемией.
Немегалобластный макроцитоз подозревается у больных с макроцитарной анемией, у которых после проведения исследований исключен дефицит витамина В12 и фолиевой кислоты. Макроовалоциты в мазке периферической крови и повышение RDW, что является типичным для классической мегалобластной анемии, могут отсутствовать. Если немегалобластный макроцитоз необъясним клинически (например, при наличии апластической анемии, хроническом заболевании печени или употреблении алкоголя) или при подозрении на миелодиплазию, необходимы выполнение цитогенетических исследований и изучение костного мозга, чтобы исключить наличие миелодисплазии. При немегалобластном макроцитозе в костном мозге мегалобласты не определяются, но при миелодисплазии и выраженном поражении печени характерны мегалобластоидные предшественники эритроцитов с плотными конденсатами хроматина, которые отличаются от обычных тонких нитей, характерных для мегалобластных анемий.
Диагностика и лечение мегалобластных анемий
Наличие мегалобластной анемии предполагается у больных с анемией и макроцитарными индексами эритроцитов. Диагноз обычно базируется на исследовании мазка периферической крови. При полной картине анемии имеет место макроцитоз с MCV > 100fl. В мазке наблюдаются овалоцитоз, анизоцитоз и пойкилоцитоз. Значение разброса эритроцитов по объему (RDW) высокое. Часто встречаются тельца Хауэлла-Жолли (фрагменты ядер). Определяется ретикулоцитопения. Рано развивается гиперсегментация гранулоцитов, позже нейтропения. В тяжелых случаях часто встречается тромбоцитопения, а тромбоциты могут иметь отклонения в размерах и форме. В неясных случаях необходимо выполнить исследование костного мозга.
Перед началом лечения должна быть установлена причина анемии. При обнаружении мегалобластной анемии предполагается наличие дефицита витамина В12 или фолиевой кислоты. При недостаточности данных, основанных на изучении периферической крови и костного мозга, необходимо определение уровня витамина В и фолиевой кислоты.
Лечение зависит от причины, вызвавшей анемию. Препараты, вызывающие мегалобластное состояние, необходимо отменить или снизить дозу.
В12 дефицитная анемия. Клиническая картина и диагностика.
Пищевые и другие причины мегалобластных анемий
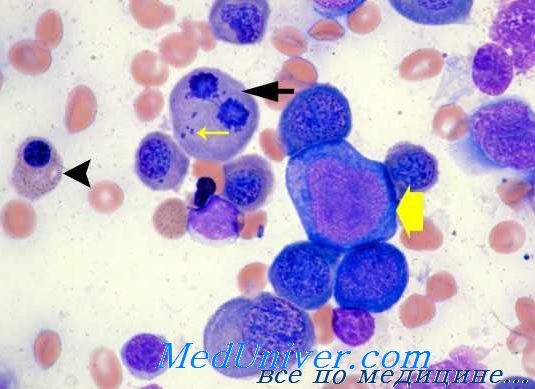
Неэффективный синтез ДНК в гемопоэтических клетках-предшественниках является основным механизмом, приводящим к мегалобластной анемии. Наиболее частыми причинами мегалобластной анемии являются дефицит витамина B12 или фолиевой кислоты. Неэффективный гемопоэз, являющийся результатом асинхронности между ядерным и цитоплазматическим развитием, наиболее очевиден на мазках аспирата костного мозга, окрашенных по Райту-Гимзе. Предшественники мегалобластных эритроидов крупнее нормальных, их ядра крупнее и кажутся незрелыми с зернистым хроматином. На начальных стадиях клеточной дифференцировки медленная конденсация хроматина приводит к образованию открытого решетчатого везикулярного ядра. На последующих этапах цитоплазмы увеличивается. количество предшественников мегалобластных эритроидов по отношению к размеру ядра. Предшественники гранулоцитов также обнаруживают ядерно-цитоплазматическую диссинхронию с развитием так называемых гигантских метамиелоцитов и полос, которые имеют характерное подковообразное ядро и открытый хроматин. На развитие мегакариоцитов также влияют аномальные большие полилобластные мегакариоциты с отсутствием цитоплазматических гранул. Соответствующие изменения в мазке крови включают анемию с овальными макроцитами, анизоцитоз, пойкилоцитоз, лейкопению с гиперсегментированными полиморфноядерными клетками и тромбоцитопению.
Патогенез мегалобластной анемии.
Анемия развивается постепенно с достаточным временем для сердечно-легочной и интраэритроцитарной компенсации до появления симптомов. Симптомы обычно развиваются у пациентов с тяжелой анемией. Основные симптомы включают слабость, сердцебиение, утомляемость, головокружение и одышку, вызванные низким гематокритом. Желтуха может возникнуть в результате интрамедуллярного и внесосудистого гемолиза. Лейкопения или тромбоцитопения обычно присутствуют, но обычно не вызывают клинических опасений. При дефиците B12 часто возникают неврологические симптомы, а также вегетативные желудочно-кишечные расстройства. Неврологические симптомы возникают в результате симметричных парестезий, онемения и нарушения чувствительности к вибрации и позе, что приводит к нарушениям походки. При дефиците B12 могут быть церебральные проявления, включая спутанность сознания, паранойю, слабоумие и даже явный психоз.13 Другие сопутствующие симптомы, редко встречающиеся при дефиците витамина B12, включают генерализованную мальабсорбцию, вызванную мегалобластозом кишечника, бесплодием, глосситом и церебральным синдромом. венозный тромбоз.
Лабораторная диагностика В12 дефицитной анемии.
Мегалобластическая анемия что это
Тиамин-зависимая мегалобластная анемия (TRMA) была впервые описана в 1969 г. Роджерсом и соавт. [1, 2]. Они выдвинули гипотезу, что причиной анемии является нарушение метаболизма витамина B1, что было эмпирически подтверждено коррекцией последней после перорального приема тиамина. Дисфункция высокоаффинного переносчика тиамина (THTR-1), ответственного за трансмембранный транспорт витамина B1, вызывает анемию, а также экстрамедуллярное повреждение (бета-клетки и клетки внутреннего уха) [3]. Редкость данного заболевания и неосведомленность медицинского персонала часто являются причиной задержки начала диагностики и лечения. Как правило, источником информации о данной патологии в научной печати являются отдельные сообщения о клинических случаях.
Патология встречается редко, в литературе описано менее ста отдельных клинических случаев [1]. Распространенность и заболеваемость доподлинно неизвестны. Большинство случаев происходит из изолированных сообществ или других общин, где распространены близкородственные связи (что объясняется аутосомно-рецессивным характером наследования). Как правило, это страны Ближнего, Среднего Востока или Центральной Азии: Иран, Турция, Индия, Пакистан. Опубликованы случаи диагностики в Китае и Японии [1, 4]. В Европе описано несколько случаев у представителей европеоидов без анамнеза близкородственных связей [1, 5].
Витамин B1 – водорастворимый витамин, который в высоких концентрациях содержится во всех тканях, особенно в скелетных мышцах, сердце, печени, почках и головном мозге. Его основная активная форма – пирофосфат тиамина. Он участвует в нескольких основных энергетических метаболических процессах: превращении пирувата в ацетил-коэнзим А в цикле Кребса (как кофактор пируватдегидрогеназы и альфа-кетоглутаратдегидрогеназы), пентозофосфатном пути (как кофакторе транскелотазы) [1, 6], и в катаболизме разветвленных аминокислот, таких как лейцин, изолейцин и валин [1, 7, 8]. Витамин B1 также играет пока не совсем ясную роль в нервной проводимости, независимо от его роли в качестве кофактора [6].
1) при физиологических концентрациях в плазме (
Мегалобластическая анемия что это
В большинстве случаев обследование больных начинается на фазе уже развитой мегалобластической анемии. Схематично оно развертывается в следующей последовательности: выявление анемии, определение ее мегалобластического характера, диагностирование дефицита витамина В12 или фолиевой кислоты (или исключение такой возможности), уточнение патофизиологического механизма недостаточности, установление нозологической единицы, в которой развился дефицит (возможно и условий, способствующих его развитию).
Отмеченная последовательность находится в обратном порядке по сравнению с последовательностью нарушений во времени; при этом, в создании дефицита названных двух витаминов различаются следующие три фазы: биохимическая (когда количество витаминов сокращается в среде организма), гематологическая (при которой возникает мегалобластоз) и клиническая (с уже определившейся анемией).
В ряде случаев причиной, вызывающей диагностическое исследование, является не анемия, а иные проявления (например, невропатия, расстройства пищеварения, мегалобластические изменения без анемии и пр.) или патологические состояния, потенциально могущие обусловить развитие соответствующих дефицитов (беременность, гемолитическая анемия, алкоголизм и пр.). Такое мероприятие проводится именно в целях своевременного выявления анемии. Вот почему приведенная выше схема исследований может измениться коренным образом.
В нижеследующем приводятся некоторые правила, которыми следует руководствоваться на различных этапах диагностического процесса.
Диагностирование мегалобластоза в принципе не сложное дело, когда заболевание предоставляется в уже полностью развитой форме. При этом учитываются костномозговые и периферические морфологические изменения с наличием признаков неэффективности эритропоэза (ранее описанных). Для постановки раннего диагноза представляют значение «незначительные» мегалобластические изменения (Hansen), которые заключаются в наличии промежуточных мегалобластов, гигантских гранулоцитов (более 5%, а возможно и 20% всех костномозговых клеток) и гиперсегментированных гранулоцитов в крови (подозрительное число 3 и 4-дольчатых клеток).
В отношении промежуточных мегалобластов необходимо учитывать артефакты, связанные с приготовлением мазка (даже и отдельные частные особенности). Гигантские миелоидные клетки развиваются при беременности, железодефицитной анемии, отдельных инфекционно-токсических состояниях и хронических заболеваниях почек, в то время как гиперсегментирование наблюдается также в качестве врожденного дефекта.
При полностью сложившегося мегалобластоза основными задачами дифференциальной диагностики являются отождествление «резкой задержки деления » (в связи с истощением запаса фолиевокислых солей или их метаболическим блокированием) при различных хронических гемолитических анемиях, также мегалобластоза — в случаях неподдающейся лечению анемии и эритремического миелоза (синдром di Guglielmo), когда, помимо обычно положительной реакции ШИК существует, в принципе, явное преобладание мегалобластических а диспластических сдвигов.
Диагностирование этиопатогенетической категории состоит, по существу, в отождествлении дефицита витамина В12 или фолиевой кислоты, критерии которого уже рассматривались. Определение витаминемии составляет наиболее точный способ, делающий возможным выявление дефицита даже на скрытой стадии; в клинике применяются также метаболические тесты.
Определение витамина В12 (в принципе в сыворотке) выявляет его понижение до менее 150 пг/мл («предел тревоги») или 100 пг/мл (явный дефицит), а иногда (при болезни Бирмера) до 20 пг/мл. «Искусственное» повышение его показателя наблюдается после инъецирования В12 при заболеваниях печени, особенно при хроническом гемобластном лейкозе. вот почему некоторые авторы отдают предпочтение определению этого витамина в эри троцитах (норма 100—300 нг/мл) (Kelly и Herbert).
Определение фолиевокислых солей в сыворотке указывает на раннее сокращение при фолиевом дефиците (до менее 3 нг/мл), равно как и при инфекциях, новообразованиях, железодефицитной анемии и пр.; неспецифический рост отмечается нередко при дефиците В12. С учетом этого предпочтительно проводить определение в цельной крови (при дефиците до 50 нг/мл; мегалобластоз появляеткх при менее 20—15 нг/мл).
Выделение с мочой метилмалоновой кислоты при дефиците В12 увеличивается до нескольких десятков мг/сутки (иногда резко, в частности в формах с невропатией), также при нарушении метаболизма пропионовой кислоты. Положительная реакция FIGlu отмечается не только у больных с фолиевым дефицитом, но также у страдающих болезнью Бирмера, заболеваниями печени, часто у беременных и пр. В процессе диагностирования использование терапевтического теста с введением физиологических доз витамина В12 (парентерально 1—5 мкг/сутки) или фолиевой кислоты (перорально 50—100 мкг/сутки) и дальнейшим наблюдением реакции ретикулоцитов — лишь в редких случаях оказывается необходимым.
В таком случае предполагается наличие выраженной анемии, что требует питания без соответствующих витаминов. Инфекции и прочие факторы могут обусловить неправильные результаты теста.
Патофизиологическое и этиологическое диагностирование проводится по данным анамнеза, клинического обследования и требуемых при этом лабораторных исследований. Так, при дифференцальной диагностике дефицита отмеченных двух витаминов анамнез, в котором значатся хроническая неполноценность питания (нередко в сочетании с алкоголизмом), повторная беременность, заболевания кишечника с преобладающим поражением тощей кишки, как и вообще желудочнокишечные расстройства с неполноценным поглощением подсказывают, в первую очередь, наличие фолиевого дефицита, в то время как иссчение желудка или подвздошной кишки и признаки нервного расстройства — говорят о наличии дефицита витамина В12.
Клиническое обследование часто усматривает в дефиците В12 признак поражения задних и боковых канатиков, в то время как симптоматология возможной невропатии алкоголиков у больного с фолиевой недостаточностью — иная. Среди лабораторных данных выявление желудочной ахилии составляет весьма важный признак, указывающий на наличие болезни Бирмера, однако, в отдельных случаях для уточнения дополнительно проводится реакция Шиллинга (например, у леченных больных).
В целях уточнения патофизиологического механизма и этиологии основного заболевания, его осложнений и сопутствующих болезней, в зависимости от случая, можно также прибегнуть к использовании ряда простых или специальных тестов, относящихся к различным медицинским специальностям.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Анемия: симптомы, степени, лечение
Анемия, или малокровие, – состояние, при котором уменьшается концентрация гемоглобина (переносчика кислорода) в крови. Часто сопровождается понижением количества эритроцитов (красных кровяных телец). Это не самостоятельное заболевание, а синдром других болезней.
Анемия у женщин диагностируется, если гемоглобин опускается ниже 120 г/л (при беременности – ниже 110 г/л), а у мужчин, если показатель понижается до 130 г/л.
При малокровии клетки и ткани не получают достаточного количества кислорода, что приводит к нарушению функционирования внутренних органов, способствует развитию других заболеваний.
Виды анемии
В зависимости от причины различают 4 группы патологии:
Известно несколько разновидностей дефицитной патологии:
Самые распространенные формы гемолитической анемии:
Вид анемии определяется врачом — терапевтом или гематологом на основе анализов крови.
Симптомы анемии
Признаки патологии зависят от ее вида и степени тяжести. Легкая форма часто протекает бессимптомно. Возможны общая слабость, повышенная утомляемость, ослабление внимания. В тяжелых случаях (при понижении гемоглобина ниже 50 г/л) может развиться ацидоз (закисление крови), сердечная недостаточность.
К общим признакам, сопровождающим все виды анемии, принадлежат:
Для железодефицитной формы характерны наличие трещин и заед в углах рта, поперечная исчерченность, слоистость и ломкость ногтей, сечение и выпадение волос, искажение вкусовых предпочтений (желание есть мел, землю), понижение артериального давления, обмороки.
При В12-дефицитной анемии человек ощущает покалывание и онемение в пальцах, чувство ползания мурашек, скованность и отечность конечностей, кожа приобретает желтоватый оттенок, а язык – малиновый, походка становится шаткой.
При апластическом малокровии в грудной области возникают колющие боли, физические усилия сопровождаются одышкой. На коже появляются мелкие кровоизлияния (петехии) в виде красной сыпи, кровоточат десны, менструации становятся длительными и обильными.
При фолиеводефицитной форме затрудняется пережевывание и глотание пищи, атрофируются слизистые оболочки ЖКТ, развивается непереносимость кислой пищи.
При постгеморрагической анемии кружится голова, понижаются давление и температура тела, учащается (но становится слабым) пульс, появляется холодный пот. Если кровотечение обильное, то возможны судороги, коматозное состояние и даже остановка сердца.
Для гемолитического малокровия характерны желтушность кожи и слизистых оболочек, потемнение мочи и кала, повышенная температура тела, увеличение размеров печени или селезенки.
При гипопластической форме усиливается кровоточивость десен, в ротовой полости образуются язвы, на коже появляются синяки, развивается тахикардия, постоянно хочется спать.
Степени анемии
В зависимости от уровня гемоглобина различают 3 степени анемии:
Причины возникновения анемии
Спровоцировать развитие анемии способны различные факторы:
Часто анемия развивается при:
В группу риска входят вегетарианцы, доноры, профессиональные спортсмены, беременные женщины.
Основная причина анемии у детей – быстрый рост, требующий усиленного питания, и несовершенство механизмов кроветворения. В результате ослабляется иммунная система, усиливается восприимчивость к инфекционным заболеваниям.
Лечение анемии
Метод терапии врач подбирает индивидуально в зависимости от причины малокровия и тяжести состояния.
При железодефицитной анемии доктор порекомендует включить в свой рацион продукты, богатые железом. При необходимости назначит железосодержащие препараты.
Если малокровие вызвано инфекцией или интоксикацией, то необходимо избавиться от возбудителя болезни и провести детоксикацию организма.
При постгеморрагической анемии следует остановить кровотечение. Дополнительно приписывают лекарства, нормализующие объем крови и количество кровяных клеток. Если возникает угроза для жизни, переливают кровь, вводят кровезаменители.
Гемолитическую анемию лечат анаболическими гормонами и глюкокортикоидами. Дополнительно назначают витамины. Если консервативное лечение оказывается неэффективным, то прибегают к операции, во время которой удаляют селезенку.
При гипопластической форме стимулируют процессы кроветворения, выполняют переливание крови, делают пересадку костного мозга.
Серповидно-клеточную анемию лечат вливанием кровезаменителей или эритроцитарной массы.