С чем реагирует масляная кислота
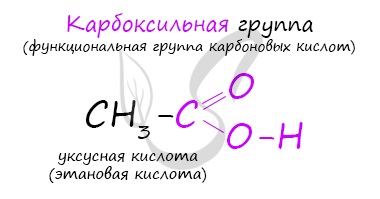
Карбоновые кислоты
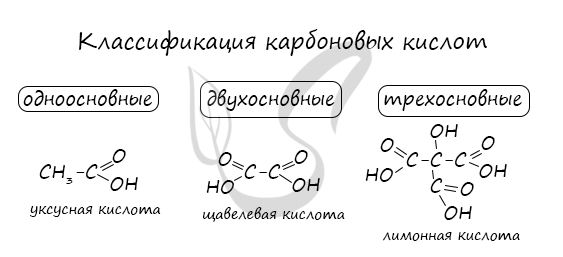
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
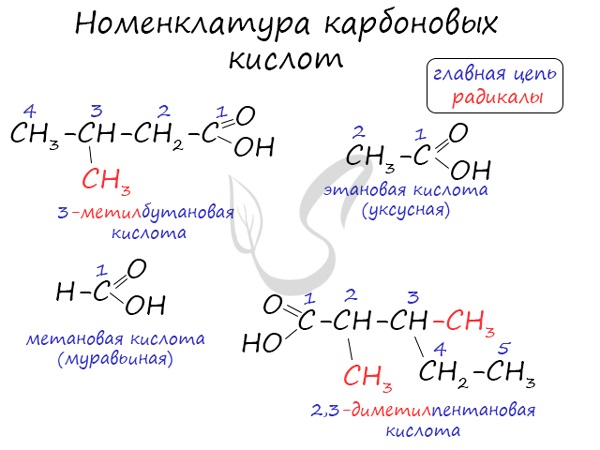
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
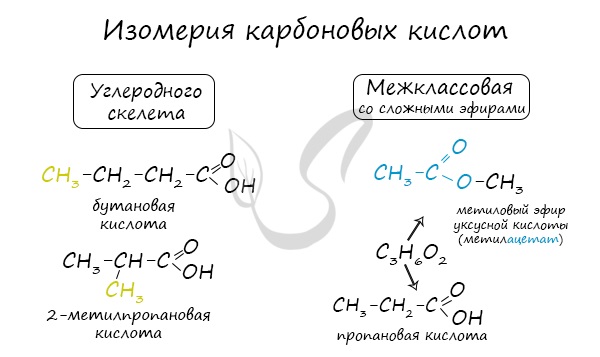
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
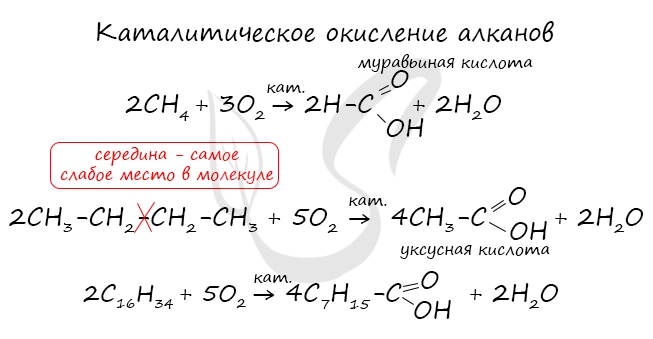
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
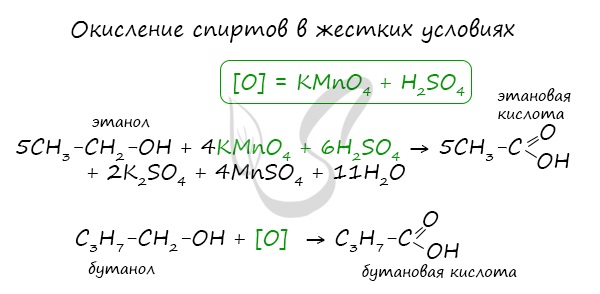
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
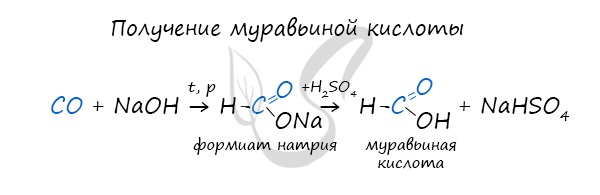
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
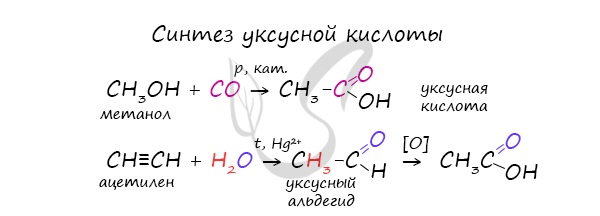
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
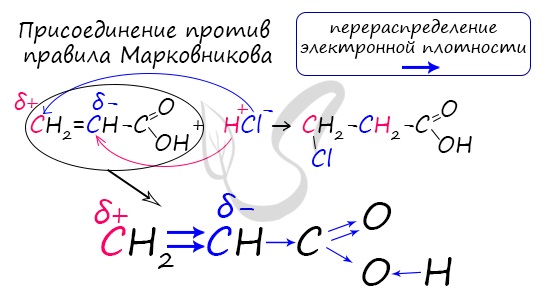
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
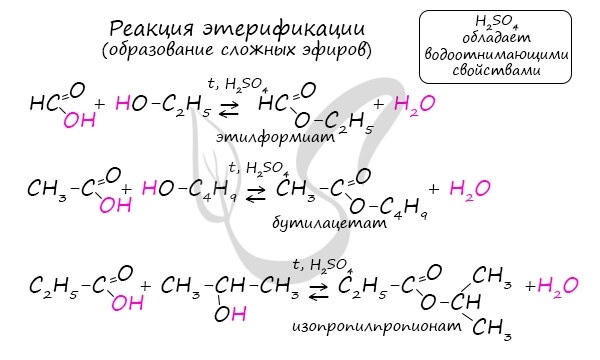
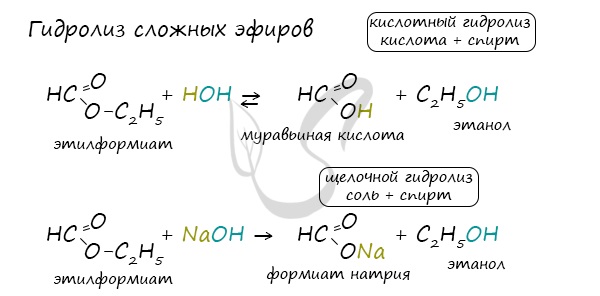
Сложные эфиры
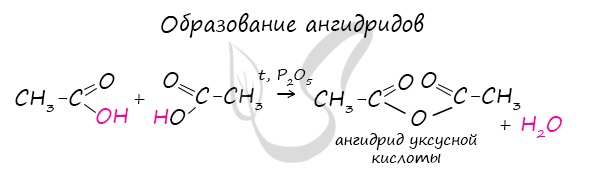
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
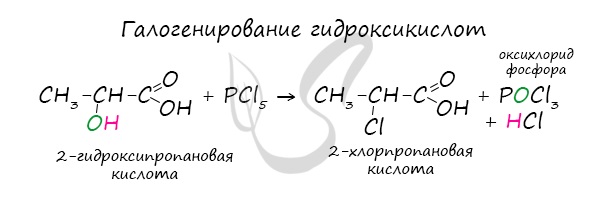
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Масляная кислота
Из Википедии — свободной энциклопедии
наименование
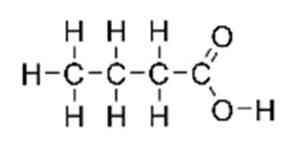
Ма́сляная кислота́ (бута́новая кислота́) СH3(CH2)2СООН — бесцветная жидкость с резким запахом прогорклого масла, которая имеет в своей структуре одну карбоксильную группу и относится к одноосновным короткоцепочечным насыщенным жирным кислотам (англ. SCFA ). Соли и сложные эфиры масляной кислоты называются бутиратами.
Масляная кислота — одна из самых важных низкомолекулярных кислот, которые синтезируются природным образом в кишечнике. Она является основным энергетическим материалом для эпителиоцитов и поддерживает кишечный гомеостаз. Также доказана корреляционная связь между дефицитом низкомолекулярных кислот и частотой развития и обострения заболеваний толстого кишечника (язвенный колит, злокачественные новообразования и др.). Масляная кислота проявляет противораковое и противовоспалительное действие, влияет на аппетит, предупреждает развитие окислительного стресса [1]
Не является основным компонентом сливочного масла, которое получают взбиванием сливок.
Формула масляной кислоты, свойства, риски и использование
масляная кислота, также известная как н-бутановая кислота (в системе IUPAC), это карбоновая кислота со структурной формулой CH3CH2CH2-COOH. Он классифицируется как жирная кислота с короткой цепью. Имеет неприятный запах, острый вкус и в то же время немного сладковатый (похож на эфир). Его структура показана на рисунке 1.
Он содержится особенно в прогорклом масле, сыре пармезан, сыром молоке, животных жирах, растительных маслах и рвоте. Его название происходит от греческого слова βουτυρος, что означает «масло» (contributors, 2016)..
Масляная кислота образуется в толстой кишке человека в результате бактериальной ферментации углеводов (в том числе пищевых волокон) и, предположительно, подавляет колоректальный рак.
Физико-химические свойства масляной кислоты
Соединение растворимо в воде, этаноле и эфире. Он мало растворим в четыреххлористом углероде. Это слабая кислота, что означает, что она не диссоциирует полностью, ее pKa составляет 4,82 (Национальный центр биотехнологической информации, S.F.).
Изомер 2-метилпропановой кислоты (изомасляной), (CH3) 2CHCO2H, найден как в свободном состоянии, так и в его этиловом эфире в нескольких растительных маслах. Хотя это коммерчески менее важно, чем масляная кислота (Brown, 2011).
Масляная кислота может реагировать с окислителями. Реакции накаливания происходят с триоксидом хрома при температуре выше 100 ° С. Они также несовместимы с основаниями и восстановителями. Может атаковать алюминий и другие легкие металлы (BUTYRIC ACID, 2016).
Реактивность и опасности
Масляная кислота считается легковоспламеняющимся соединением. Несовместим с сильными окислителями, алюминием и большинством других металлов, щелочами, восстановителями (Royal Society of Chemistry, 2015).
Соединение очень опасно в случае контакта с кожей (может вызвать ожоги), при проглатывании, попадании в глаза (раздражение) и вдыхании (может вызвать сильное раздражение дыхательных путей).
Распыленная жидкость или туман могут вызвать повреждение тканей, особенно слизистых оболочек глаз, рта и дыхательных путей..
Вещество токсично для легких, нервной системы, слизистых оболочек. Повторное или длительное воздействие вещества может вызвать повреждение этих органов, а также раздражение дыхательных путей, приводящее к частым приступам бронхиальной инфекции (паспорт безопасности материала масляная кислота, 2013 г.).
В случае попадания в глаза следует проверить, есть ли у жертвы контактные линзы, и снять их. Глаза жертвы следует промывать водой или физиологическим раствором в течение 20-30 минут, одновременно вызывая больницу.
В случае контакта с кожей пораженный участок следует погрузить в воду, одновременно снимая и изолируя всю загрязненную одежду. Аккуратно промойте все пораженные участки кожи водой с мылом. Медицинская помощь должна быть получена.
В случае вдыхания, вы должны оставить загрязненный участок в прохладном месте. При появлении симптомов (например, хрипы, кашель, одышка или жжение во рту, горле или в груди), обратитесь к врачу..
В случае проглатывания не следует вызывать рвоту. Если пострадавший находится в сознании и у него нет судорог, следует ввести один или два стакана воды, чтобы разбавить химическое вещество и вызвать больницу или токсикологический центр..
Если жертва находится в конвульсии или без сознания, не давайте ничего внутрь, убедитесь, что дыхательные пути жертвы открыты, и поместите жертву сбоку, опустив голову ниже тела. Необходимо немедленно обратиться к врачу.
Использование и польза для здоровья
Низкомолекулярные сложные эфиры масляной кислоты, такие как метилбутират, имеют запах и вкус, обычно приятные. Из-за этого они находят применение в качестве пищевых и парфюмерных добавок..
Бутират, конъюгированное основание масляной кислоты, может быть найдено в нескольких продуктах. Он также может быть добавлен в качестве добавки или ароматизатора в других.
Сложные эфиры масляной кислоты или бутираты используются для изготовления искусственных ароматизаторов и эссенций растительного масла. Бутиламират является основным ингредиентом абрикосового масла, а метилбутират можно найти в ананасовом масле..
Помимо использования в качестве ароматизатора, ананасовое масло также используется для стимулирования роста костей, лечения стоматологических операций и лечения простуды, ангины и острого синусита, в соответствии с производителем натуральных продуктов OCA Brazil (PULUGURTHA, 2015).
Исследование, опубликованное в ноябрьском выпуске «Журнала питания» за ноябрь 2010 года, указывает на то, что употребление в пищу злаков в ночное время, богатых неусвояемыми углеводами, может повысить концентрацию бутирата плазмы на следующее утро..
Он добавляет, что это может быть механизм, с помощью которого цельное зерно помогает предотвратить диабет и болезни сердца.
Масляная кислота, как и бутират, образуется в толстой кишке человека как продукт ферментации волокон, и это считается фактором, объясняющим, почему диеты с высоким содержанием клетчатки защищают от рака толстой кишки..
Было рассмотрено несколько гипотез о возможном механизме этих взаимоотношений, в том числе о том, важен ли бутират для поддержания нормальной фенотипической экспрессии эпителиальных клеток или для улучшения удаления поврежденных клеток посредством апоптоза..
Другие преимущества масляной кислоты или бутирата:
Масляная кислота
| Масляная кислота | |
 | |
 | |
| Общие | |
|---|---|
| Традиционные названия | масляная кислота |
| Химическая формула | C3H7COOH |
| Физические свойства | |
| Состояние | прозрачная жидкость |
| Молярная масса | 88,1051 г/моль |
| Плотность | 0,9563 г/см³ |
| Термические свойства | |
| Т. плав. | −5 °C |
| Т. кип. | 163 °C |
| Давление пара | 0,9 hPa |
| Классификация | |
| Рег. номер CAS | 107-92-6 |
| SMILES | CCCC(=O)O |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Масляная кислота (Бутановая кислота, Этилуксусная кислота) — одноосновная насыщенная карбоновая кислота алифатического ряда, бесцветная жидкость с запахом прогорклого масла, имеющая формулу CH3CH2CH2COOH.
Содержание
[править] Физические свойства
Масляная кислота имеет молярную массу = 88,1051 г/моль, плотность = 0,96 г/см³, температуру плавления = −5 °C, температуру кипения = 163 °C.
[править] Химические свойства
Масляная кислота растворима в воде, смешивается с органическими растворителями. Образует азеотропную смесь с водой (температура кипения = 99,4 °С, 18,4% по массе масляной кислоты).
Соли и эфиры масляной кислоты называются бутиратами.
Например, бутират натрия получают по формуле:
Химические свойства масляной кислоты типичные для карбоновых кислот, например при взаимодействии со спиртами происходит реакция этерификации (реакция проводится в присутствии катализатора, обычно в качестве катализатора для этой реакции используется серная кислота H2SO4), например реакция с метанолом СН3ОН даёт метиловый эфир масляной кислоты и воду:
[править] Практическое применение
Данная кислота содержится в небольших количествах в коровьем масле (3-4%) и нефти. В промышленности получают каталитическим окислением масляного альдегида или бутанола (окислением изомасляного альдегида или изобутилового спирта), а также сбраживанием сельскохозяйственных отходов, содержащих крахмал.
Масляную кислоту и изомасляную кислоту применяют в качестве экстрагента щелочноземельных металлов (Са, Sr, Mg, Ba) при очистке от них редкоземельных элементов, для обеззоливания (удаление солей Са), например при декальцинировании кож; в синтезе душистых веществ для парфюмерии, ароматизирующих веществ в пищевой промышленности (метилбутират имеет запах яблока, изоамилбутират — запах груши), пластификаторов для лаков на основе эфиров целлюлозы, эмульгаторов, ацетобутирата целлюлозы, служащего основой для атмосфероустойчивых покрытий, бутирилхолингалогенидов (субстраты для выявления холинэстеразы).
Для масляной кислоты ПДК = 10 мг/м³. Необходимо не допускать попадания масляной кислоты на кожу и глаза. Данная кислота при попадании в водоёмы токсична для водных организмов.
Бутановая кислота
Масляная кислота (бутановая кислота) С3Н7СООН – бесцветная жидкость с запахом прогорклого масла. Соли и эфиры масляной кислоты называются бутиратами.
Масляная кислота и её эфиры содержатся в коровьем масле и нефти. Эфиры масляной кислоты применяют как душистые вещества, пластификаторы, эмульгаторы; масляная кислота – в производстве ацетобутиратов целлюлозы.
Масляная кислота образуется при маслянокислом брожении:
Масляная кислота имеет два изомера:
Одноосновные предельные карбоновые кислоты
Полезное
Смотреть что такое «Бутановая кислота» в других словарях:
Изобутановая кислота — н бутановая кислота изобутановая кислота Масляная кислота (бутановая кислота) С3Н7СООН – бесцветная жидкость с запахом прогорклого масла. Соли и эфиры масляной кислоты называются бутиратами. Масляная кислота и её эфиры содержатся в коровьем масле … Википедия
Жирная кислота — Жирные кислоты (алифатические кислоты) многочисленная группа исключительно неразветвлённых одноосновных карбоновых кислот с открытой цепью. Название определяется, во первых, химическими свойствами данной группы веществ основанными на присутствии… … Википедия
МАСЛЯНАЯ КИСЛОТА — (бутановая к та, этилуксусная к та) СН 3 СН 2 СН 2 СООН. В статье рассмотрена также изомасляная к та (2 метилпропановая к та, диметилуксусная к та) (СН 3)2 СНСООН (И. к.). Мол. м. 88,11; бесцв. жидкости, М. к. с запахом прогорклого масла. Для М.… … Химическая энциклопедия
Одноосновные предельные карбоновые кислоты — (одноосновные насыщенные карбоновые кислоты) карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH Номенклатура Систематические названия… … Википедия
Насыщенные монокарбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
Одноосновные насыщенные карбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
Предельные монокарбоновые кислоты — Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой COOH. Все они имеют общую формулу СnH2n+1COOH, где n … Википедия
Жирные кислоты — алифатические одноосновные карбоновые кислоты с открытой цепью, содержащиеся в этерифицированной форме в жирах, маслах и восках растительного и животного происхождения. Жирные кислоты, как правило, содержат неразветвленную цепь из четного числа… … Википедия
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
Карбоновые кислоты — Карбоновые кислоты класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп COOH. Кислые свойства объясняются тем, что да … Википедия