сосудистый паркинсонизм код по мкб 10
Сосудистый паркинсонизм
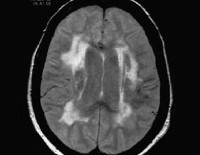
Сосудистый паркинсонизм — это уменьшение числа, амплитуды и скорости произвольных движений на фоне мышечной ригидности, этиопатогенетически связанное с наличием цереброваскулярной патологии. Клинически проявляется медлительностью, шаркающей походкой, постуральной неустойчивостью, гипомимией лица, склонностью к депрессии. Сосудистый генез заболевания устанавливается на основании данных УЗДГ интра- и экстракраниальных сосудов, церебральной нейровизуализации. Лечение преимущественно консервативное, состоит из базовой (сосудистой) и симптоматической (антипаркинсонической) терапии.
МКБ-10
Общие сведения
Впервые предположение о наличии сосудистого фактора среди прочих причин поражения чёрной субстанции высказал в 1894 году французский невролог Бриссауд. В 1929 году американским врачом М. Критчли было представлено первое подробное описание атеросклеротического паркинсонизма. С внедрением в практическую неврологию методов нейровизуализации в России в 1997 году были разработаны клинико-нейровизуализационные критерии диагностики, модифицированные в 2004 году. Сосудистый паркинсонизм (СП) относится к редким формам вторичного паркинсонизма и составляет, по различным данным, 2-15% от всех его случаев. Патология диагностируется у 11% пациентов, перенёсших ишемический инсульт, в 14% случаев подкорковой формы ДЭП. Средний возраст больных колеблется в диапазоне 40-90 лет.
Причины
Основным этиологическим фактором развития СП выступает поражение подкорковых ганглиев, обусловленное цереброваскулярными нарушениями. Последние могут иметь острое (инсульт, лакунарный инфаркт) и хроническое (хроническая ишемия головного мозга) течение. Заболевание чаще возникает вследствие патологических изменений, происходящих в церебральных артериях на фоне хронической артериальной гипертензии. С учетом калибра поражённых сосудов выделяют две основные группы этиофакторов:
Патогенез
Патологические изменения малых мозговых артерий потенцируют диффузную гипоперфузию тканей. Повышенная проницаемость стенок поражённых сосудов вызывает периваскулярный отёк, отложение гемосидерина, выход белков плазмы за пределы сосудистого русла. Результатом хронической ишемии и сосудистой проницаемости является гибель подкорковых структурных элементов. Погибшие участки недостаточно замещаются астроцитами, что становится причиной спонгиоза — патологической губчатости белого вещества.
Поражение крупных ветвей и ствола средней церебральной артерии (сосудистый стеноз, окклюзия, истончение стенки) провоцирует возникновение инсульта с образованием обширного участка некроза подкорковых элементов. Таким образом, сосудистый фактор приводит к гибели дофаминпродуцирующих нейронов, дисметаболизму дофамина, повреждению дофаминовых рецепторов. Преобладание ацетилхолиновых активирующих воздействий на тормозящее моторику хвостатое ядро ведёт к гипокинезии, развивается паркинсонизм.
Классификация
Сосудистый паркинсонизм имеет вариабельную клиническую картину, может сочетаться с иными неврологическими симптомами, связанными с гемодинамическими изменениями, вторичными дегенеративными процессами. Указанные факторы обуславливают определённые диагностические трудности. Разобраться в многообразии клинической симптоматики помогает выявление характерных особенностей течения СП. В соответствии с данным критерием выделяют три варианта:
Особенности течения заболевания в значительной мере коррелируют с характером цереброваскулярной патологии. Понимание этиологии возникновения СП имеет определяющее значение для адекватного планирования лечебных мероприятий. В связи с этим целесообразно выделение следующих двух форм:
Симптомы сосудистого паркинсонизма
В типичных случаях отмечается двустороннее подострое развитие симптоматики. Гипокинезия, мышечная ригидность преобладают в нижних конечностях. Пациенты жалуются на скованность, затруднения при ходьбе, «прилипание ступней к полу». Походка замедленная, шаркающая, мелкими шажками. Типична медлительность, отсутствие жестикуляции, обеднение мимики. Рано появляется постуральная неустойчивость — дискоординация, затрудняющая удержание тела в определённой позе и при изменении положения. Мышечная ригидность приводит к постоянному полусогнутому положению конечностей.
В ряде случаев заболевание манифестирует появлением лёгких паркинсонических знаков: изолированной олигобрадикинезии (в пределах нижних конечностей), одного умеренно выраженного симптома паркинсонизма, нескольких проявлений лёгкой степени. Симптоматика начальной стадии суммарно не достигает определяющих истинный паркинсонизм критериев, аналогична дебюту ряда дегенеративных заболеваний, клинике возрастных подкорковых изменений. Заподозрить СП в подобных случаях можно по мере прогрессирования симптомов.
Сосудистый паркинсонизм протекает без нарушений обоняния (аносмии). Характеризующий болезнь Паркинсона тремор покоя выявляется лишь в 4% случаев СП. Сопутствующая симптоматика зависит от локализации и распространённости сосудистого поражения. Чаще наблюдаются пирамидные расстройства, мозжечковая атаксия, в дебюте заболевания маскирующие паркинсонизм. Возможны тонические расстройства, миоклонии, псевдобульбарный синдром, симптомы очагового поражения высших нервных функций (афазия, амнезия, апраксия), лобный синдром. Типично прогрессирующее интеллектуальное снижение.
Осложнения
Ранее формирование постуральных расстройств значительно затрудняет самостоятельные передвижения пациента, опасно падениями, травмированием больного. Ситуация усугубляется при наличии мозжечковых и пирамидных нарушений. Ограничение двигательной активности осложняется формированием контрактур суставов. Сопровождающие паркинсонизм изменения личности (сужение круга интересов, замкнутость, пониженный фон настроения) способствуют возникновению депрессии. Прогрессирующие когнитивные расстройства ведут к деменции. Больной утрачивает возможность самообслуживания, требует постоянного ухода. Псевдобульбарный паралич опасен аспирацией пищи с развитием аспирационной пневмонии.
Диагностика
Диагностировать сосудистый паркинсонизм врачу-неврологу позволяет наличие клинических критериев акинетико-ригидного синдрома, подтверждённого инструментальными исследованиями цереброваскулярного заболевания, выявления причинно-следственной связи между ними. Поскольку сосудистый генез патологии обуславливает полиморфизм клинических проявлений, устанавливать диагноз СП целесообразно, если паркинсонизм является доминирующим синдромом. Основные диагностические мероприятия включают:
Важное место в диагностическом поиске занимает дифференциальная диагностика. Особую сложность представляют пациенты пожилого возраста, поскольку у них часто обнаруживаются сосудистые нарушения и возрастная дегенерация базальных ганглиев. Дифференцировать сосудистый паркинсонизм от болезни Паркинсона позволяют особенности течения, отсутствие постурального тремора, расстройств обоняния, наличие пирамидной, мозжечковой сопутствующей симптоматики. Значительные сложности представляет дифдиагностика сосудистой патологии от дегенеративных поражений ЦНС (мультисистемной атрофии, деменции с тельцами Леви, кортикобазальной дегенерации). Достоверно исключить первично-дегенеративный генез подкорковых нарушений можно только на основе данных патоморфологического анализа.
Лечение сосудистого паркинсонизма
Терапия СП требует комплексного подхода, направленного на лежащий в основе патологии этиопатогенетический фактор и основные клинические проявления заболевания. Существенное значение имеет нормализация мозговой гемодинамики, профилактика возникновения ОНМК. В большинстве случаев применяется консервативное лечение, включающее:
Хирургическое лечение сводится к стереотаксическим операциям. Наиболее распространена паллидотомия — частичное разрушение бледного шара. Вмешательство может быть эффективным при ограниченных поражениях. Многоочаговые процессы, а также экстранигральный, не связанный с патологией чёрной субстанции паркинсонизм плохо поддаются нейрохирургическому лечению.
Прогноз и профилактика
Эффективность лечения СП зависит от этиологии цереброваскулярных расстройств, локализации и обширности поражения. Компенсировать проявления паркинсонизма удаётся у пациентов с положительным ответом на терапию леводопой. Локализация поражения в стриарной и таламической областях обуславливает резистентный к дофаминовой терапии паркинсонизм, имеющий более серьёзный прогноз.
Первичная профилактика СП включает исключение факторов, приводящих к патологическим изменениям сосудов головного мозга (курения, атерогенного питания, набора избыточной массы тела), адекватную коррекцию артериальной гипертензии, своевременную терапию сердечно-сосудистых заболеваний. Вторичная профилактика заключается в поддержании полноценной мозговой гемодинамики, профилактике острых нарушений церебрального кровотока. Пациентам под наблюдением терапевта или кардиолога следует осуществлять постоянный контроль артериального давления. Рекомендованы регулярные курсы сосудистой терапии.
Сосудистый паркинсонизм код по мкб 10
Потребность в классификации любой группы заболеваний определяется необходимостью более четкого понимания их структуры, их природы, особенностей клинических проявлений, возможностью прогнозировать их течение, разработки более рациональных и эффективных подходов к их лечению.
Развитие клинической неврологии было тесно связано с созданием и развитием топической диагностики поражений нервной системы. Успехи топической диагностики всегда были предметом профессиональной гордости клинических неврологов. Однако при изучении патологии базальных ганглиев традиционные представления о топической диагностике не подтвердились: попытки связать клинические проявления экстрапирамидных расстройств с поражением определенных структур базальных ганглиев оказались безуспешными.
Примером такой попытки может служить работа Jörg Baumann (1963), который предложил выделять в группе экстрапирамидных расстройств следующие клинико-топические синдромы: 1) палеостриарный синдром (т.е. поражение бледного шара), к которому относили болезнь Паркинсона, другие болезни с синдромом паркинсонизма, болезнь Галлервордена–Шпатца и эссенциальный тремор; 2) неостриарный синдром (т.е. поражение хвостатого ядра и скорлупы), который проявляется разными формами гиперкинезов и дискинезий – болезнь Гентингтона, другие формы хореи, разные формы дистонии; 3) оливоруброцеребеллярный синдром (совокупность поражения структур «топографического церебрального треугольника», включающего системы красных ядер, олив и мозжечка), при котором наблюдается миоклоническая диссинергия Ханта [4].
В нашей стране в те же годы свои подходы к классификации экстрапирамидных расстройств предложил Л.С.Петелин. Применяя анатомо-патофизиологический подход, он систематизировал гиперкинезы в соответствии с уровнем поражения структур головного мозга. Он писал: «Такой подход дает возможность определить структуру гиперкинеза в зависимости от физиологических параметров моторных центров разных уровней нервной системы» [3]. При этом он выделял: 1) гиперкинезы стволового уровня (все виды органического тремора, паркинсонический тремор покоя, миоклонии, стереотипии); 2) гиперкинезы преимущественно подкоркового уровня (хорея, атетоз, торсионная дистония, баллизм); 3) подкорково-корковые гиперкинезы (разные формы миоклонии).
Таблица 1. Нейронные круги обратной связи ядер экстрапирамидной системы и синдромы нарушения функции нейронных колец (по Л.С.Петелину, 1970)
| Нейронное кольцо | Структуры мозга, объединенные в нейронное кольцо | Неврологические синдромы при нарушении функции кольца |
| I | 8, 6 и 4-е поля коры – стриопаллидум – таламус – кора | Хореоатетоз и торсионная дистония |
| II | Кора – стриопаллидум – нигроретикулярные структуры – таламус – кора | Паркинсоническое дрожание и другие виды тремора |
| III | Руброталамические – дентаторубральные образования | Интенционное дрожание |
| IV | Кора – стриопаллидум – красное ядро – олива – зубчатое ядро – таламус – кора | Миоклонии |
Анализ своей гипотезы и данных других авторов позволил ему предложить схематическое изображение возможного взаимодействия центров экстрапирамидной системы разного уровня [2]. В такой схеме описывались нейронные круги и выделялись синдромы нарушения функции 4 нейронных колец при экстрапирамидных расстройствах (табл. 1).
Однако анатомо-клинические классификации не нашли практического применения. Сложность вопроса классификации экстрапирамидных расстройств лежит еще и в плоскости терминологических понятий. Экстрапирамидные расстройства связывают с патологией базальных ганглиев, которые традиционно рассматривают как подкорковые узлы в глубоких отделах полушарий головного мозга.
В то же время формально термин «экстрапирамидные структуры» предполагает, что к ним могут быть причислены все образования и системы вне пирамидной кортикоспинальной системы: мозжечковая, вестибуло- и ретикулоспинальная, а также такие структуры, как зрительный бугор, красные ядра и черная субстанция, которые формально не относятся ни к пирамидной системе, ни к базальным ганглиям. Более того, теперь хорошо известно, что основные эфферентные пути, несущие импульсы от базальных ганглиев, пройдя через зрительный бугор, направляются к клеткам коры, чтобы принять участие в формировании пирамидного пути. На протяжении этого пути волокна двух систем смешиваются и следуют вместе, за исключением ограниченного участка – пирамид продолговатого мозга, в которых волокна пирамидной системы следуют изолированно. Таким образом, термины «экстрапирамидные структуры» и «экстрапирамидные расстройства» носят условный характер.
Как писал П.Мильнер (1973), «само подразделение моторной системы на пирамидную и экстрапирамидную является источником путаницы и ошибок. Возможно, следствием исторического заблуждения является представление, что пирамидная система является единственной двигательной системой. Поэтому те отделы мозга, участие которых в двигательной функции было выявлено позднее, были объединены под названием „экстрапирамидная система“. Трудно провести четкую функциональную грань между этими системами. Не обособлены они и анатомически, за исключением короткой части пути через продолговатый мозг» [1].
Один из основоположников современного учения об экстрапирамидной патологии, американский невролог S.Fahn, создавая в 1968 г. специализированную клинику для пациентов с болезнью Паркинсона, принял решение, что в этой клинике также будут находиться больные с разными формами нарушения движений, как с гипокинетическими (паркинсонизм, пластическая мышечная ригидность), так и с гиперкинетическими формами (гиперкинезы, разные формы дистонии и дискинезии). Он назвал свое отделение «клиника для больных с нарушением движений» (movement disorders clinic). Это название тоже имело очевидное условное ограничение, так как S.Fahn не предполагал включать в эту группу больных с другими нарушениями движений: при пирамидных парезах и спастичности, а также больных с поражением мотонейронов передних рогов серого вещества спинного мозга. Однако, как показало время, предложенное название – «нарушение движений» – вписалось в современную неврологическую терминологию. Теперь с таким названием функционируют национальные и региональные общества неврологов, собираются конгрессы и конференции, издаются журналы [5].
Первая и единственная масштабная попытка создать общепризнанную классификацию экстрапирамидных расстройств была осуществлена под эгидой Всемирной федерации неврологии специальной комиссией, созданной по инициативе американского невролога профессора Melvin D. Yahr, председателя секции экстрапирамидных расстройств Всемирной федерации неврологии той поры. В комиссию входили всемирно известные неврологи: Andre Barbeau (Канада), Roger C. Devoisin (США), Franz Gerstenbrandt (Австрия), C.D.Marsden (Великобритания). Эта комиссия под председательством профессора Johannes P.W.F. Lakke (Нидерланды) опубликовала в 1981 г. доклад «Классификация экстрапирамидных расстройств. Предложения для международной классификации и глоссария терминов» [12]. Обращает на себя внимание деликатное замечание авторов в названии – они называют свою работу «предложения для классификации и глоссария», т.е. не навязывают свое мнение всем специалистам и считают возможными коррекционные дополнения. Тем не менее авторы дали детальное описание и оценку разных форм нарушения движений. В классификации экстрапирамидных расстройств были выделены 2 части: часть 1 – классификация и номенклатура в описании экстрапирамидных расстройств; часть 2 – степень тяжести двигательных нарушений.
К числу очевидных достоинств этой классификации можно отнести: 1) выделение первичных форм как идиопатических спорадических, так и наследственных экстрапирамидных заболеваний; 2) выделение вторичных (симптоматических) форм, имеющих не дегенеративную природу, а определенно иную (часто известную) причину поражения мозга; 3) оценку степени тяжести проявлений двигательных нарушений и дефицита объема повседневной активности в условных количественных единицах (баллах); 4) рекомендации клинических приемов и определенных тестов для объективного выявления нарушений; 5) создание глоссария.
Со времени опубликования классификации прошло более 30 лет, однако за прошедшее с тех пор время ни за рубежом, ни в нашей стране этот доклад не послужил толчком к дискуссии специалистов-неврологов. В то же время не было ни одного выступления с критикой указанной классификации. К профессиональной чести членов авторской группы можно отнести тот факт, что они были самокритичны [6]. В предисловии к докладу этой комиссии сказано, что авторы «отдали приоритет симптому», т.е. рассматривают свою классификацию как симптоматическую. Можно полагать, что симптом представляет собой слишком узкий и изолированный элемент клинической картины, чтобы быть основанием для выработки подходов к нозологической диагностике. Чтобы убедиться в некорректности симптоматического подхода, достаточно рассмотреть один пример из этой классификации. Согласно предложенной в этой классификации структуре систематизации экстрапирамидных расстройств, одна из наиболее распространенных нозологических форм – болезнь Паркинсона – «расходится» по трем разным разделам классификации: гипокинезия – раздел IA, тремор – раздел – IB, ригидность – раздел IID1. Эта очевидная нелепость препятствует применению такой классификации для нозологической диагностики экстрапирамидных расстройств. Второе наше замечание: мы считаем некорректным объединение в общую группу «первичных» форм как при моносиндромных моносистемных, так и при полисиндромных мультисистемных вариантах экстрапирамидных расстройств. При таком подходе принятая авторами как важнейший «объединяющий» признак «первичность» затушевывает очевидные различия моно- и мультисистемных форм [8]. В последние десятилетия мультисистемные формы на практике для краткости именуют «синдром-плюс», что обозначает наличие в комбинированном синдроме признаков поражения не только экстрапирамидной, но и других систем. Например, к формам «паркинсонизм-плюс» относят прогрессирующий надъядерный паралич и мультисистемную атрофию [9, 11].
В недавние годы наряду с традиционными клиническими формами экстрапирамидных расстройств в эту группу были включены и некоторые другие заболевания с нарушениями движений. Это нашло отражение в «феноменологической» классификации нарушений движений, предложенной тремя выдающимися неврологами (S.Fahn, C.D.Marsden, J.Jankovic, 2011) (табл. 2). Однако она, на наш взгляд, не является в строгом понимании классификацией, а представляет собой только перечень экстрапирамидных расстройств. Она не может служить подспорьем в постановке нозологического диагноза.
Таблица 2. Классификация расстройств движений [10]
* В оригинальном тексте у авторов перечень терминов нарушений движений дан в соответствии с порядком алфавита английского языка. Этот порядок сохранен при переводе.
В свете изложенного выше мы считаем, что наиболее рациональна клиническая синдромологическая классификация, которая систематизирует экстрапирамидные расстройства на основании доминирующего клинического синдрома: паркинсонизма, тремора, мышечной дистонии, хореи, тика, миоклонии, атетоза, пароксизмальных форм дискинезии, других гиперкинезов. Практическому неврологу нужен путеводитель, «дорожная карта», чтобы не заблудиться в «дебрях» экстрапирамидных расстройств при постановке диагноза и по возможности правильно назвать заболевание, которое послано на грешную душу его больного.
Дорога к диагнозу экстрапирамидного расстройства бывает трудна и извилиста. Местами она напоминает топкое болото. И чтобы преодолеть это «болото», нужно знать, что в нем есть спасительные «твердые кочки». Чтобы преодолеть болото, нужно уметь прыгать с одной опорной кочки на другую, а чтобы не засосала трясина, нужно держать в руках спасительную слегу (длинную жердь). Вот такой «кочкой» и «слегой», которые помогают неврологу, мы видим клиническую синдромологическую классификацию экстрапирамидных расстройств [7, 8].
Системный подход к нозологическому диагнозу экстрапирамидных расстройств предполагает выделение в каждом из этих синдромов трех этиологических групп заболеваний:
Таблица 3. Клиническая классификация паркинсонизма
| Этиологическая категория | Основные нозологические формы | Код МКБ-10 |
| Первичный паркинсонизм | Болезнь Паркинсона | G20 |
| Юношеский паркинсонизм | G23.8 | |
| Вторичный (симптоматический) паркинсонизм | Лекарственный паркинсонизм | G21.1 |
| Посттравматический паркинсонизм | G21.2 | |
| Токсический паркинсонизм | G21.2 | |
| Постэнцефалитический паркинсонизм | G21.3 | |
| Паркинсонизм при гидроцефалии | G21.8/G22* | |
| Сосудистый паркинсонизм | G21.8/G22* | |
| Паркинсонизм при других дегенеративных заболеваниях ЦНС («паркинсонизм-плюс») | Преимущественно спорадические формы | |
| Мультисистемная атрофия | G23.2/G90.3 | |
| Прогрессирующий надъядерный паралич | G23.1 | |
| Болезнь диффузных телец Леви | G23.8 | |
| Кортикобазальная дегенерация | G23.8 | |
| Гемипаркинсонизм-гемиатрофия | G23.8 | |
| Болезнь Альцгеймера | G30†/G22* | |
| Болезнь Крейтцфельдта–Якоба | A81.0†/G22* | |
| Наследственные формы | ||
| Болезнь Гентингтона | G10 | |
| Спиноцеребеллярные дегенерации | G11.2 | |
| Нейродегенерация с накоплением железа | G23.0 | |
| Гепатолентикулярная дегенерация | Е83.0 | |
| Паллидарные дегенерации | G23.8 | |
| Семейная кальцификация базальных ганглиев | G23.8 | |
| Нейроакантоцитоз | G23.8 |
К этой группе принадлежат заболевания, которые могут быть наследственными (например, дистония, болезнь Гентингтона) или спорадическими (например, болезнь Паркинсона).
(спорадические и наследственные) заболевания ЦНС. В этих случаях помимо экстрапирамидной симптоматики выявляются признаки, связанные с поражением других систем ЦНС, например: пирамидный синдром, мозжечковая атаксия, вегетативная недостаточность. В целом заболевания этой группы представляют собой мультисистемные дегенерации. Место для заболевания с первичным полисиндромным и мультисистемным проявлением в клинической синдромологической классификации определяется дебютным и/или преобладающим синдромом. Часть из них имеет наследственный характер (например, спиноцеребеллярные дегенерации), другие – преимущественно спорадические (например, мультисистемная атрофия или прогрессирующий надъядерный паралич), но и здесь следует подчеркнуть условность границы между наследственными и спорадическими формами. К этой же группе мы относим и наследственные метаболические заболевания ЦНС (например, гепатолентикулярная дегенерация), при которых, в отличие от вышеупомянутых болезней, известен метаболический субстрат. Предлагаемую клиническую синдромологическую классификацию предлагаем рассмотреть на примере синдрома паркинсонизма (табл. 3).
По такому алгоритму в клинической синдромологической классификации представлены и другие экстрапирамидные синдромы [5, 6].