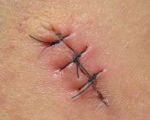
воспаление послеоперационного шва код мкб
Послеоперационная серома ( Серома шва )
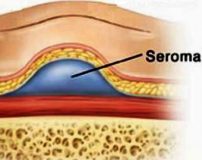
Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
МКБ-10
Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.
Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.
Гнойная костная патология
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Лечение
Консервативная терапия применима при негнойном (серозно-инфильтративном) остром гематогенном остеомиелите – антибиотики широкого спектра действия.
Предпочтительны антибактериальные препараты 3-го и 4-го поколения из группы цефалоспоринов (цефтриаксон), аминогликозидов (амикацин) и препараты из группы фторхинолонов (офлоксацин, ципрофлоксацин, пефлоксацин).
Учитывая высокую вероятность развития сепсиса, консервативную терапию целесообразно ограничить конкретным периодом, только в течение 24 часов с момента установления диагноза негнойного ОГО. Затем при отсутствии эффекта выполнить лечебно-диагностическую трепанацию кости, и в случае обнаружения высокого внутрикостного давления, независимо от характера экссудата, дополнительно дренировать костномозговой канал с установлением в нем аспирационно-промывной системы. Выявленная флегмона потребует широкой (окончатой) трепанации.
Операция независимо от обнаружения изолированного внутрикостного абсцесса, флегмоны костномозгового канала или деструкции кости предусматривает полную некрэктомию и полноценное дренирование очага воспаления. Объем резекции кости зависит от протяженности и глубины поражения мягких структур кости и кортикального слоя, от декомпрессивной трепанации в виде одного или нескольких фрезевых отверстий с последующим аспирационно-промывным дренированием до широкой, окончатой трепанации-резекции с последующим тампонированием раны.
Опыт лечения таких больных показывает необходимость выполнения послеоперационных перевязок-ревизий раны в течение 1-2 недель под общим обезболиванием, что позволяет завершить полноценность некрэктомии.
Следует отказаться от длительного повторного консервативного лечения ХГО в любом виде (антибактериальная, физиотерапевтическое и прочие терапии). Как исключение оно применимо при некоторых первично-хронических формах ХГО.
Следует настойчиво добиваться полного выздоровления пациента, так как с течением времени эффективность оперативного лечения снижается, появляются осложнения местного (дерматиты, раки и др.) и общего (амилоидоз) характера.
Консервативную терапию проводят в объеме, необходимом для подготовки к операции (повышение резистентности организма, нормализация гомеостаза, снижение «активности» воспаления в кости и окружающих тканях). Нет необходимости стандартизировать этот этап лечения, так как выбор лекарственных средств, способов физиотерапии и т.д. индивидуален.
В течение 2-3 недель больной готовится к операции. «Предоперационную» антибиотикотерапию не применяем. Исключения составляют случаи обострения ХГО, когда угроза сепсиса представляется реальной.
Для того чтобы стандартизировать оперативный метод (основа хирургии остеомиелита) лечения ХГО различных локализаций (плоские, губчатые и крупные трубчатые кости), по-видимому, следует признать единство терминологии применительно к характеру операции, и совершенно (определенно) обоснованно выделить: паллиативные, условно-радикальные и радикальные операции.
Достичь 100% выздоровления больных после условно-радикальных операций (фистулосеквестрнекрэктомия, остеонекрэктомия, резекция кости и т.д.) не представляется возможным. И это не зависит от «современных» дополнительных способов оптимизации и повышения эффективности оперативного метода (лазерное выпаривание, ультразвуковая кавитация, системы дренажей, УФО крови и другие способы и средства).
Деформации скелета, укорочения конечности и анкилозы, нередко сопровождающие радикальные (и условно-радикальные) операции, не следует рассматривать как отрицательный результат, ибо в лечении ХГО главным остается избавление пациента от хронической пиогенной инфекции и предупреждение амилоидоза. Ортопедические коррекции после выздоровления от ХГО минимизируют оперативные (и связанные с самой болезнью) последствия. Реальным и необходимым остается совершенствование условно-радикальных операций.
При наличии гнойных послеоперационных осложнений, связанных с внутренними и внешними ортопедическими протезными устройствами, имплататами и трансплататами, после полного обследования больного определяется тактика оперативного лечения: удаление вышеуказанных устройств, секвестрнекрэктомия или тотальная резекция остеомиелитического очага с последующим замещением образовавшейся костной полости или дефектов костной ткани мышечными, костными или синтетическими трансплантатами, моно- или билокальным чрескостным остеосинтезом, дренирование операционной раны, с применением местных длительно рассасывающихся антибактериальных препаратов.
В предоперационном периоде во время операции и после проводится антибактериальная терапия с учетом чувствительности микрофлоры (цефалоспорины 3-4 поколения, аминогликозиды, фторхинолоны, метронидазол, противогрибковые препараты), инфузионная дезинтоксикационная терапия (например, гемодез, физ. раствор, кристаллоиды), средства стабилизирующие гемодинамику и улучшающее микроциркуляцию (рефортан, стабизол, реополиглюкин, и др.), гемотрансфузии (эритроцит. масса, СЗП, антистафилококковая плазма, тромбомасса, криопреципитат), дезагреганты, антикоагулянты (прямого и непрямого действия), средства, улучшающие тканевой обмен (солкосерил, витамины группы В, А, С, Е), гормонотерапия (анаболики, глюкокортикоиды).
Индикаторы эффективности лечения: восстановление целостности костной ткани без наличия остеомиелитической полости, купирование явлений остеомиелита.
* – препараты, входящие в список основных (жизненно важных) лекарственных средств.
Другие уточненные послеродовые инфекции
Рубрика МКБ-10: O86.8
Содержание
Определение и общие сведения [ править ]
Раневую инфекцию в акушерстве принято подразделять на раневую инфекцию в области промежности и нижних отделов родовых путей, а также инфекцию в области разреза на передней брюшной стенке.
Этиология и патогенез [ править ]
Раневой процесс разделяется на 3 основные фазы:
— расплавления некротизированных тканей и очищения раны;
— регенерации (образования грануляционной ткани);
В каждой из этих фаз возможно развитие раневой инфекции. Патогенез раневого процесса, описываемый как взаимодействие локальных и системных реакций, на сегодняшний день окончательно не уточнен.
Клинические проявления [ править ]
При редкой клостридиальной раневой инфекции основной жалобой больных являются постоянно усиливающиеся непереносимые давящие боли в пораженной области. Состояние больных быстро ухудшается: прогрессирует общая слабость, бледность кожных покровов, усиленное потоотделение, нарастает тахикардия, снижается артериальное давление, может развиться септический шок. Рана при осмотре резко болезненна, нет гиперемии и гноетечения, характерных для других инфекционных процессов; покрыта серым налетом; отделяемое серозное желто-коричневое с неприятным запахом, отек тканей прогрессивно увеличивается, расширяется зона некроза, при пальпации краев раны определяется крепитация.
Другие уточненные послеродовые инфекции: Диагностика [ править ]
Факторы риска раневой инфекции передней брюшной стенки включают хориоамнионит, ожирение или истощение, сахарный диабет, лечение кортикостероидами, продолжительное или экстренное хирургическое вмешательство.
Кроме общих факторов риска для всех послеродовых гнойно-воспалительных заболеваний, можно выделить ряд специфических факторов, характерных для данного осложнения:
— специфические и неспецифические кольпиты и цервициты;
— несоблюдение правил личной гигиены;
— нарушение правил обработки раны промежности и на передней брюшной стенке в послеродовом периоде;
— технические погрешности при хирургическом восстановлении целостности ран промежности или передней брюшной стенки: дефекты гемостаза (гематома), продолжительная операция, большая кровопотеря, нарушение анатомических соотношений при сопоставлении краев раны.
Диагностика раневой инфекции возможна уже на основании появления местных классических клинических симптомов:
— гиперемия (эритема) вокруг раны;
— местное повышение температуры;
— локализованный болевой синдром;
— серозное, сукровичное или гнойное отделяемое из раны.
• Клинический анализ крови: выявляется лейкоцитоз с увеличением числа сегментоядерных нейтрофилов, лимфопения, анемия.
• Биохимический анализ крови: часто выявляется гипопротеинемия, повышение содержания билирубина и печеночных ферментов.
• Микробиологическое исследование раневого отделяемого: забор производят стерильным ватным тампоном до обработки раны антисептическими растворами.
• Ультразвуковое исследование (УЗИ) находит широкое применение для неинвазивной диагностики воспалительных процессов мягких тканей, выявления гематом различной локализации и полостей.
• Рентгенологическое исследование зоны очага поражения при анаэробной инфекции позволяет подтвердить наличие газа в мягких тканях и его распространение по ходу магистральных сосудов
• Пункции с последующим исследованием пунктата необходимы для диагностики флегмон и абсцессов мягких тканей. Диагноз инфекционного очага может быть идентифицирован только при получении во время пункции гнойного содержимого.
• Лапароскопическое исследование используется при подозрении на перитонит.
• Компьютерная и магнитно-резонансная томография дают возможность топически диагностировать тазовые абсцессы, флегмоны забрюшинного пространства, малого таза и т.д.
Дифференциальный диагноз [ править ]
Необходимо различать стафилококковую, стрептококковую, грамотрицательную и анаэробную раневую инфекцию для выбора оптимальной антибактериальной терапии.
Другие уточненные послеродовые инфекции: Лечение [ править ]
Для лечения раневой инфекции используют хирургические методы очищения раны и антибактериальную терапию. Кроме этого применяются иммуно- и реокорригирующие средства, а также эфферентные методы лечения. Лечебная тактика должна определяться фазой раневого процесса. Действие применяемого метода лечения должно соответствовать особенностям фазы раневого заживления. Если в I фазе необходимо обеспечить антимикробное, некролитическое, сорбирующее, обезболивающее и защитное действие, то во II и III фазах следует создать условия для оптимального течения репаративных процессов.
Главные цели лечения сводятся к комплексному воздействию на основные факторы, способствующие развитию раневой инфекции, замедлению течения фаз раневого процесса и заживлению раны.
Показания к госпитализации
Все случаи раневой инфекции требуют лечения в условиях стационара.
Важным компонентом лечения раневой инфекции является антибиотикотерапия, которая должна быть назначена до хирургического лечения с целью создания необходимой бактерицидной концентрации в зоне раны, чтобы препятствовать диссеминации инфекции во время оперативного вмешательства. До получения сведений об антибиотикочувствительности выделяемых микроорганизмов из раны используют эмпирическую антибактериальную терапию.
При ограниченном поражении с целью купирования острого гнойного процесса достаточно использование одного антимикробного препарата, назначаемого парентерально, с обязательным местным лечением гнойной раны под повязками с лекарственными средствами, обладающими широким спектром антимикробной активности (например, левосин, левомеколь, 5% диоксидиновая мазь и др.).
При обширных гнойных очагах, осложнившихся сепсисом, необходимо использовать максимальные дозы антибиотиков парентерально или их комбинации.
Продолжительность системной антибиотикотерапии в зависимости от тяжести раневой инфекции может составлять от 3-5 до 10-14 и более дней. Ранняя отмена антимикробной терапии до достижения стойкого клинического эффекта может привести к рецидиву или затяжному течению болезни.
Показано также применение цефалоспоринов, которые имеют однонаправленный с пенициллинами механизм бактерицидного действия, но превосходят последние по антибактериальной активности. Цефалоспорины I поколения (цефазолин) являются антибиотиками узкого спектра действия, их целесообразно рассматривать в качестве базовых антибиотиков для профилактики и лечения инфекций средней тяжести. В более тяжелых случаях применяют цефалоспорины II и III поколений (цефамандол, цефокситин, цефуроксим, цефтриаксон, цефотаксим, цефтазидим). Цефалоспорины II поколения обладают широким спектром антимикробного действия, они значительно превосходят препараты первого поколения по активности в отношении грамотрицательных возбудителей. Цефалоспорины III поколения имеют менее широкий спектр действия, чем цефалоспорины II поколения, зато отличаются более выраженным эффектом в отношении определенных групп грамотрицательных аэробов и анаэробных микроорганизмов. Так как цефалоспорины не обладают достаточной эффективностью против энтерококков, при подозрении на данную инфекцию необходимо использовать ингибиторозащищенные пенициллины.
При тяжелой форме раневой инфекции целесообразно проводить комбинированную антибактериальную терапию:
— ингибиторозащищенные пенициллины или цефалоспорины III поколения + аминогликозиды;
— цефалоспорины поколения + нитроимидазолы (метронидазол) или линкозамиды (клиндамицин, линкомицин);
В современных условиях наиболее эффективными препаратами для монотерапии при тяжелых формах инфекции являются карбапенемы (имипенем/циластатин, меропенем). Активность карбапенемов против широкого спектра патогенных микроорганизмов делает их особенно эффективным при проведении монотерапии полимикробных и смешанных аэробно-анаэробных инфекций, первичной терапии до определения бактериальных возбудителей при раневой инфекции, осложненной сепсисом.
Помимо антибактериальных препаратов в комплекс лечения раневой инфекции необходимо включать инфузионную терапию при интоксикации и гипертермии, противогрибковые препараты для системного применения, антигистаминные препараты, иммуномодуляторы. При тяжелых формах раневой инфекции рекомендуется плазмаферез, УФО крови, озонотерапия и другие эфферентные методы терапии.
Профилактика [ править ]
Задачи неспецифической профилактики решаются в период предоперационной подготовки больных и выполнения оперативного вмешательства. К ним относятся:
— нормализация гомеостаза и обмена веществ;
— ликвидация сопутствующих очагов инфекции;
— обеспечение сокращения предоперационного периода пребывания больного в стационаре;
— ограничение числа присутствующих в операционной;
— качественная обработка кожи антисептиками;
— совершенствование техники операции;
— тщательный гемостаз, сокращение времени операции.
Прочее [ править ]
Раневая инфекция встречается достаточно редко, при адекватном проведении комплексного лечения опасности для здоровья женщины не представляет.
Хирургическое лечение больных послеоперационным медиастинитом и остеомиелитом грудины и ребер
Общая информация
Краткое описание
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ХИРУРГИЧЕСКОМУ ЛЕЧЕНИЮ БОЛЬНЫХ ПОСЛЕОПЕРАЦИОННЫМ МЕДИАСТИНИТОМ И ОСТЕОМИЕЛИТОМ ГРУДИНЫ И РЕБЕР (Краснодар-Москва 2014)
Определение
Стерномедиастинит – это инфекционное осложнение, возникающее после рассечения грудины, с вовлечением в инфекционный процесс костной ткани грудины, тканей средостения, с вовлечением/без в процесс поверхностных мягких тканей, с наличием/без стабильности грудины. (Инфекция в хирургии, №2,2009 Вишневский А.А. и соавторы; Complications of midlaine sternothomy Robiscek F., section 5, Pearson s thoracic & esofageal surgery, 2008).
Несостоятельность шва грудины после срединной стернотомии в сочетании с присоединившейся инфекцией расценивается как стерномедиастинит (СМ), поскольку составляющими раны являются органы и клетчатка средостения, а также грудная кость, ребра и мягкие ткани передней грудной стенки. В отдельных случаях, когда пациенты не получают должного объема хирургического лечения, болезнь принимает рецидивирующий и затяжной характер, принося немалые страдания (Софроний С.В.,1992).
Код МКБ 10
Формулируя диагноз у больного с осложнениями, развившимися после стернотомии, подлежащего лечению в хирургической клинике, необходимо использовать код в соответствии с классификацией МКБ-10, а также указывать осложнения, требующие хирургической коррекции (МКБ-10).
M86.3 Хронический многоочаговый остеомиелит
M86.6 Другой хронический остеомиелит
J98.5 Болезни средостения, не классифицированные в других рубриках
J85.3 Абсцесс средостения
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Классификация
Раневые осложнения после полной срединной стернотомии варьируют от стерильного расхождения краев раны до гнойного медиастинита.
Приведенная ниже классификация по El Oakley & John E. Wright (1996) основывается на сроках манифестации осложнения, наличии факторов риска и неэффективных попыток хирургического лечения (таблица 2).
Таблица 2. Классификация медиастинита 1 по El Oakley & John E. Wright, 1996
| Тип | Характеристика |
| I | Возникает в первые 2 недели п/о периода при отсутствии факторов риска 2 |
| II | Возникает в период от 2 до 6 недель п/о периода при отсутствии факторов риска 2 |
| IIIa | Медиастинит I типа при наличии 1 или более факторов риска |
| IIIb | Медиастинит II типа при наличии 1 или более факторов риска |
| IVa | Медиастинит I, II или III типа после одной неэффективной попытки лечения 3 |
| IVb | Медиастинит I, II или III типа после более чем одной неэффективной попытки лечения |
| V | Возникает позже 6 недель после операции |
1 – инфекция грудной стенки, ассоциированная с остеомиелитом грудины с/без инфицирования ретростернального пространства.
2 – факторы риска, установленные в 3 или более крупных исследованиях. В настоящее время таковыми признаны: сахарный диабет, ожирение и прием иммуносупрессоров.
3 – неэффективная попытка лечения включает любое хирургическое вмешательство, направленное на лечение медиастинита.
Некоторые авторы подразделяют инфекционные осложнения со стороны стернотомной раны (SWI, sternal wound infection) на две группы: поверхностные SWI с поражением лишь кожи и подкожно-жировой клетчатки и глубокие SWI с развитием остеомиелита грудины в сочетании с инфицированием ретростернального пространства или без него (Omran A.S., Karimi A., Ahmadi S.H. et al., 2007).
В свою очередь, Вишневский А.А., Рудаков С.С. и Миланов Н.О. с соавторами (2005) полагают, что термин «послеоперационный стерномедиастинит» является собирательным, так как инфицирование грудины почти всегда сопровождается поражением ребер, хрящей, мышц грудной стенки, ключиц, переднего средостения.
Диагностика
Выявление клинических симптомов, характерных для раннего расхождения шва грудины, при осмотре врача как в стационаре, так и при обращении в первичную сеть к специалистам любого профиля, требует дальнейшего целенаправленного осмотра хирурга-специалиста и выполнения назначенного им дообследования пациента для подтверждения или исключения несостоятельности грудины (уровень доказательности А).
1. Данные анамнеза. Выяснение анамнестических данных и изучение предыдущих медицинских документов является началом диагностического процесса у данной категории больных
2. Подробный физикальный осмотр в перевязочной и взятие биоматериала для бактериологического посева. Пациент тщательно осматривается в перевязочной, производится забор отделяемого и биоптата из раны на микрофлору и чувствительность к антибиотикам, проводится оценка степени поражения, функциональные особенности грудино-реберного каркаса в условиях патологического процесса.
3. ЭКГ, Эхо-КГ, ФВД (по показаниям: проба с физической нагрузкой, суточное ЭКГ-мониторирование)
4. Компьютерная томография органов грудной клетки с реконструкцией грудины (при отсутствии возможности – обзорная рентгенография органов грудной клетки).
5. ОАК, БХК + СРБ, коагулограмма, прокальцитониновый тест (по показаниям).
6. Осмотр специалистов по показаниям (кардиолог, пульмонолог, невролог, нефролог и тд.).
7. Ультразвуковое исследование раны
8. Фистулография (при наличии свищей)
Неоспоримо значимым из методов диагностики является мультиспиральная компьютерная томография (МСКТ) грудной клетки. Данное исследование легко переносится больными и является высокоинформативной методикой в диагностике инфекционно-воспалительных заболеваний грудины и рёбер. Современный мульти- спиральный компьютерный томограф имеет высочайший уровень разрешения, способен воспроизводить картинку в формате 3D – объемное изображение, выполнять послойную реконструкцию тканей, органов и структур, а также производить компьютерную ангиографию сосудов, в том числе селективную.
Кроме того, ценность этого метода состоит в том, что при восстановлении картины заболевания пациента на мониторе, врач может произвести виртуальную операцию, просмотрев индивидуальные анатомические особенности пациента и патологических процессов протекающих у него. Совпадения виртуальной операции с обычной хирургической составляют 88% [Vogel H., Nagele B., Arnold P. J.].
Мы отмечаем необходимость проведения компьютерной томографии не только до операции, но и после неё, с целью контроля состояния костных структур раны, оценки радикальности выполненной резекции, отсутствия гематом. Так как инфекционно-воспалительные заболевания склонны к рецидивированию, КТ обоснованно применять в отдаленные сроки.
С помощью ультразвукового метода исследования можно определить локализацию и форму патологического очага в грудной стенке, выявить наличие и расположение жидкостного компонента – гематом, абсцессов [50, 53,54].
Лечение
Лечение больного со стерномедиастинитом должно быть комплексным и мультдисциплинарным.
Хирургическое лечение
Первичная (вторичная) хирургическая обработка гнойной раны.
Основной метод лечения воспалительных заболеваний грудной стенки – хирургический, этапный [13,21,25,33,43,50,68].
На первом этапе производится хирургическая обработка раны с ревизией и удалением наложенных ранее швов и резекцией некротических участков как костных структур, так и мягких тканей. Во время операции из вскрытых очагов некроза, гнойных затеков производится забор материала на исследование микрофлоры и чувствительность к антибактериальным препаратам.
Таблица 3
«Стартовая» антибиотикотерапия (до получения результатов посевов, с учетом наиболее частых возбудителей) – эртапенем 1 г 1 раз в сутки или пиперациллин/тазобактам 4,5 г 4 раза в сутки; при высокой вероятности MRSA (10-15%) – к лечению добавляется ванкомицин, или линезолид, или телаванцин. При высокой вероятности ESBL-продуцентов используются карбапенемы или тигециклин. («Справочник по антимикробной терапии» Козлов Р.С., Дехнич А.В., 2013). Дальнейшая коррекция антибактериальной терапии должна проводиться согласно результатам посевов и чувствительности к антибиотикам.
Проводимое местное лечение претерпевает изменения согласно результатам микробиологического исследования раневого отделяемого, получаемого во время каждой перевязки при использовании вакуумной терапии или 1 раз в 3 дня при использовании мазевого метода.
На третьем этапе лечения выполняются операции с целью ликвидации дефекта передней грудной стенки (пластический этап).
Варианты реконструктивных операций:
1. Реостеосинтез грудины с применением рутинного шва грудины стальной лигатурой или с применением современных имплантов и фиксирующих систем: Z|ipFix, монофиламентной нити, имплантов из металла с памятью формы и др.
2. Пластика мышечным лоскутом. Возможно использовать: большую и малую грудные мышцы, прямую мышцу живота, широчайшую мышцу спины.
3. Пластика прядью большого сальника. При избыточном объеме сальника возможно выполнение частичной резекции пряди для создания трансплантата необходимой величины.
Способ проведения трансплантата на грудную стенку к области реципиентного участка зависит, главным образом, от конфигурации стернальной раны и сообщения с лапаротомной раной. Перемещение пряди производится по раневому каналу, соединяющему раны грудной и брюшной стенок и через подкожный «тоннель» или через диафрагмотомию.
При питающей ножке небольшого диаметра и близком расположении переднего края диафрагмы к стернальной ране возможно проведение сальника через крестообразную диафрагмотомию. При этом трансплантат проводят в одной из «слабых» зон диафрагмы – ретростернальном пространстве. Способ наиболее предпочтителен в отношении профилактики формирования в отдаленных сроках послеоперационной диафрагмальной грыжи в области проведения питающей ножки.
Перемещенный БС целесообразно фиксировать по контуру раны отдельными узловыми швами, укрывая края резецированных грудины и ребер. Операцию необходимо завершить дренированием брюшной полости, пространств над и под перемещенным лоскутом.
По окончании транспозиции пряди сальника в реципиентную область на передней грудной стенке, рана ушивается узловыми широкозахватными неишемизирующими швами.
Большой сальник, обладая высоким иммунологическим и пластическим эффектом, совмещая эти две функции, остается универсальным пластическим материалом в торакальной и пластической хирургии (уровень доказательности С).
Наблюдение и лечение пациента предпочтительнее проводить в условиях реанимационного отделения с целью максимально эффективного мониторинга, диагностики, коррекции лечения и протезирования витальных функций.
Ранние послеоперационные осложнения
Несостоятельность шва мягких тканей передней грудной стенки, кровотечение, подтвержденное поступлением крови по ретро- и антестернальным дренажам.
Поздние послеоперационные осложнения
Рецидив гнойного процесса в ране, болевой синдром, дискомфорт в проекции передней грудной стенки, послеоперационные вентральные и диафрагмальные грыжи.
Что нельзя делать
1. При установлении диагноза послеоперационный медиастинит – нельзя откладывать хирургическое лечение и надеяться на консервативную терапию;
2. Нельзя оперировать пациента с некомпенсированной коагулопатией;
3. Нельзя выполнять хирургическую обработку раны без адекватного анестезиологического пособия;
4. Нельзя оставлять нефиксированные отломки грудины и ребер в ране;
5. Нельзя частично «сводить» грудину, средостение должно быть открыто полностью;
6. Нельзя игнорировать мобилизацию внутренней части грудины от переднего средостения;
7. Нельзя укладывать губку на сердце без предварительного отграничения неадгезивным сетчатым перевязочным материалом (см. выше);
8. Нельзя выполнять реконструктивную операцию без достижения всех необходимых для этого критериев;
Дальнейшее ведение, обучение и реабилитация пациента
Пациенты, перенесшие реостеосинтез грудины либо резекционно-пластические операции на грудине, обязаны соблюдать строгие ограничения физической нагрузки в течение 6 месяцев:
1. ограничить движение в поясе верхних конечностей (не поднимать руки выше плечевого пояса);
2. исключить несимметричные физические нагрузки на верхний плечевой пояс;
3. ношение эластического бандажа на грудную клетку;
Медикаментозная терапия заключается в лечении сопутствующих заболеваний, согласно рекомендациям соответствующих специалистов.
Прогноз
Летальность у пациентов со стерномедиастинитом варьирует от 14 до 47% (Franco S. et аl., 2009)
При условии раннего выявления, своевременной хирургической помощи и комплексного подхода в лечении, прогноз для жизни пациента благоприятный.
Пациенты, перенесшие обширные резекционные костные операции, инвалидизируются до уровня II группы инвалидности.
В 4-7% случаев у пациентов могут развиваться хронические свищевые формы остеомиелита ребер и грудины, в последующем требующие соответствующего этапного хирургического лечения.
Профилактика
Оценка факторов риска – залог минимизации осложнений
Развитие осложнений после срединного трансстернального доступа многие авторы описывают у пациентов, входящих на предоперационном этапе в так называемую «группу риска» [12,18,19,84,119,131]. Факторы риска возможного развития осложнений после срединной стернотомии делятся на предоперационные, интраоперационные и послеоперационные (таб.1).
Предоперационными «факторами риска» являются хронические нарушения обмена веществ (ожирение, сахарный диабет), обострения хронических заболеваний легких (ХОБЛ, астма), нарушения работы выделительной системы (хроническая почечная недостаточность), снижение иммунологической реактивности организма, длительный прием лекарственных препаратов, снижающих свертываемость крови, прием стероидных гормонов, препаратов комплексного лечения гипертонической болезни [12,55, 66,119]
Интраоперационными «факторами риска» являются значительная кровопотеря [79,118,128,129], продолжительность операции, время искусственного кровообращения (ИК) [12,71,84], компрессия (ишемия) в зоне операционной раны. Выделяют риск развития воспалительного процесса при наличии гематом [71,83,102,120,128], по существу, являющихся инкубатором для бактерий. Кроме этого, среди причин осложнений, в литературе есть указания на использование медицинского воска, вызывающего образование гранулем в области шва грудины [2,15,31,34,133].
Послеоперационными «факторами риска» являются нестабильность грудины, ишемия сосудов грудины, прорезывание швов грудины, кровотечение, рестернотомии, продолжительная ИВЛ, непрямой массаж сердца, низкий сердечный выброс, респираторный дистресс-синдром, иммунодепрессия, неправильное ведение больного в послеоперационном периоде, декомпенсация хронических заболеваний [55,71,79,102,128,132].
Таблица 1. Факторы риска, приводящие к развитию стерномедиастинита
| Предоперационные факторы риска | Интраоперационные факторы риска | Послеоперационные факторы риска |
| Хронические заболевания (ИБС, ХОБЛ, ХПН, СД и др.) Прием ГКС Иммунодефицит Деформация грудной клетки Почечная недостаточность Длительное использование диуретиков Остеопороз Курение, ХОБЛ Рестернотомии Индекс массы тела > 30 | Метод пересечения грудины Неправильная дистракция раны Поперечный перелом грудины Метод ушивания грудины Шовный материал Продолжительность операции Длительное ИК (> 2 часов) Массивная кровопотеря Бимаммарное шунтирование Несрединная стернотомия Внутриаортальная баллонная контрпульсация Симультанная операция Техника хирурга | Анемия, требующая гемотрансфузии (Hb |
Интраоперационная профилактика включает:
1. АБТ профилактика – повторное введение дозы антимикробного препарата при длительности операции больше двух периодов полувыведения препарата, выбранного для профилактики.
2. Хирургические мероприятия:
• Обработка операционного поля хлоргексидином 3-х кратно
• Рассечение мягких тканей, включая надкостницу скальпелем
• Технически симметрично выполненная стернотомия
• Скелетирование внутренних грудных артерий
• Промывание раны и полости перикарда теплым стерильным физиологическим р-ром
• Раздельное дренирование перикарда и ретростернального пространства
• Исключение применения воска для гемостаза грудины
• Стабилизация грудины 6-8 восьмиобразными швами
• Ушивание фасциально-мышечного слоя отдельными швами. Подкожная жировая клетчатка не ушивается
• Ушивание кожи внутрикожным швом мононитью на режущей игле
3. OFF-pump хирургия (по возможности).
4. Анестезиологические мероприятия:
• Внутривенные линии находятся на большом расстоянии от пациента
• Введение препаратов осуществляется на большом расстоянии от центрального венозного катетера.
(«Элиминация стернальной инфекции в кардиохирургии» П.Р. Фогт, Г.Г. Хубулава, 2012)
Информация
Источники и литература
Информация
Академик РАМН В.А. Кубышкин, член-корреспондент РАМН В.А. Порханов
Координаторы работы:
Научный совет: В.А. Кубышкин, В.Д. Паршин, В.А. Порханов
Состав рабочей группы по разработке рекомендаций:
В.А. Порханов, А.А. Печетов, В.А. Митиш, А.А. Звягин, А.Л. Коваленко, Г.Г. Кармазановский, И.А. Косова, С.А. Бурякина
Список сокращений:
БС – большой сальник
ЖС – желудочно-сальниковая (артерия)
ОГ – остеомиелит грудины
КТ – компьютерная томография
МРТ – магнитно-резонансная томография
ИБС – ишемическая болезнь сердца
АКШ – аортокоронарное шунтирование
МКШ – маммарокоронарное шунтирование
ОИМ – острый инфаркт миокарда
МК – митральный клапан
АК – аортальный клапан
ТК – трикуспидальный клапан
ВГА – внутренняя грудная артерия
СД – сахарный диабет
СМ – стерномедиастинит
VAC – вакуумная повязка
NPWT – низковакуумное раневое лечение
Off-pump – без искусственного кровообращения
SSWI – неглубокая (поверхностная) раневая инфекция
DSWI – глубокая стернальная раневая инфекция