код диагноза по мкб с44
Код диагноза по мкб с44
К первичным опухолям наружного носа относятся базально-клеточный рак, плоскоклеточный рак, меланома. Старческая кератома и пигментная ксеродерма отнесены к группе предраковых заболеваний. Кератоакантома по существу является доброкачественной опухолью, однако дифференцировать ее от плоскоклеточного рака очень трудно.
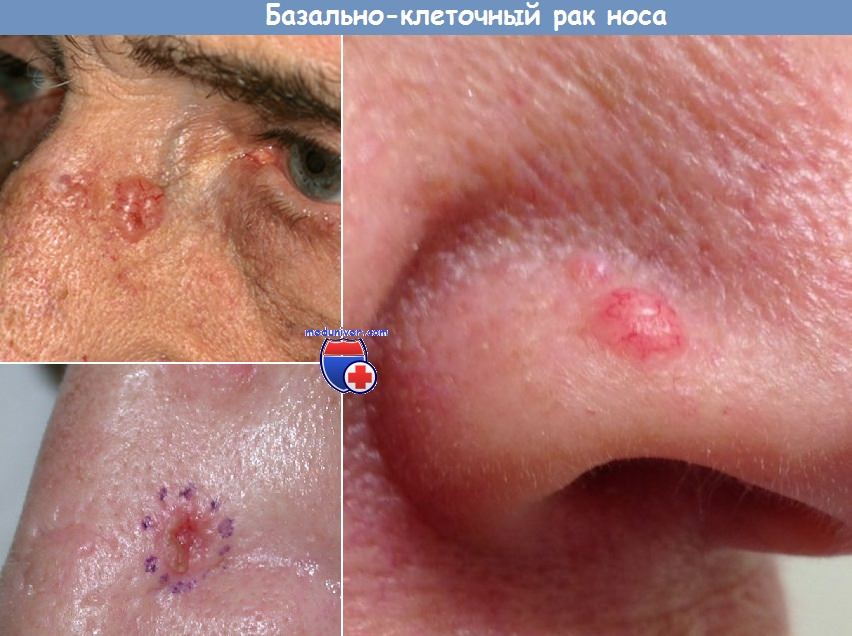
а) Клиническая картина. Опухоль вначале имеет вид небольшого одиночного узелка с телеангиэктазией. В центральной части узелка часто отмечается ямка, которая медленно увеличивается в размере. Позднее узелок изъязвляется и инфильтрирует поверхностные слои подлежащих тканей.
Базальноклеточный рак одинаково часто встречается у мужчин и у женщин, возраст больных, у которых обнаруживают эту опухоль, составляет 60-70 лет. У 70% больных опухоль на момент диагностики не превышает в диаметре 1 см, но часто отмечается значительное распространение опухоли на окружающие ткани, и она занимает площадь, превышающую 20 см2. Истинный базально-клеточный рак не метастазирует, и переход в плоскоклеточный рак наблюдается очень редко.
Однако в опухоли, которая ранее была облучена или удалена недостаточно радикально, могут развиться дистрофические изменения, и она становится очень агрессивной, распространяясь гематогенно в другие части тела (например, в легкие).
Различают следующие клинические формы базально-клеточного рака:
• нодулярную: выпуклый лоснящийся узелок, часто имеется ямка в центральной части;
• язвенную: отмечается изъязвление базально-клеточного рака, опухоль имеет вид узелка с плоской язвой на нем;
• инвазивную: характеризуется быстрым ростом и значительным прорастанием в окружающие ткани;
• склеродермоподобную: атрофические изменения в опухоли, которая окружена четкообразным ободком и прорастает в дерму;
P.S. Границы распространения опухоли всегда больше, чем определяются при клиническом обследовании.
• поверхностную: плоская, увеличивающаяся в размерах шелушащаяся бляшка, часто светло-коричневого цвета с четкообразным валиком на периферии.
б) Диагностика. Наиболее часто базально-клеточный рак локализуется в центральной части лица и на ушной раковине. Если имеются сомнения в диагнозе, выполняют биопсию (трепанобиопсия).
в) Дифференциальный диагноз. Плоскоклеточный рак и предраковые изменения.
г) Лечение базально-клеточного рака носа. Методом выбора является полное иссечение опухоли с гистологическим контролем.
Первичное лечение состоит в полном иссечении опухоли с гистологическим исследованием краев препарата. Образовавшийся дефект временно закрывают аллотрансплантатом (синтетический заменитель кожи) и после гистологического подтверждения полноты удаления опухоли выполняют реконструктивную операцию местными тканями, например ротационными или перемещенными лоскутами либо свободным трансплантатом.
В отдельных случаях при поверхностной форме базально-клеточного рака проводят лучевую терапию, местную иммунотерапию имиквимодом (5% мазь) или фотодинамическую терапию.
Операция по Мосу. Фредерик Мос (1910-2002) в 1941 г. описал технику удаления опухолей кожи. Операция Моса состоит в ступенчатом удалении кожи тонкими слоями с немедленным микроскопическим контролем краев иссекаемой опухоли. Преимущество этого метода в том, что он позволяет выполнять контролируемую резекцию опухоли и раневой поверхности при минимальном объеме резецируемой ткани. Для микроскопического исследования используют замороженные срезы.
д) Прогноз базально-клеточного рака носа. Если опухоль удается удалить полностью, прогноз благоприятный. Полноту удаления опухоли контролируют путем гистологического исследования краев удаляемых срезов, при необходимости увеличивая глубину резекции. Базально-клеточный рак метастазирует лишь с развитием в опухоли дистрофических изменений.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Стади рака кожи
Чем отличаются 1, 2, 3 и 4 стадии рака кожи? Как развивается рак кожи? Как сильно пострадал организм? Как растут метастазы при этом виде онкологии и какие органы они поражают? Как расшифровать медицинские диагнозы?
Диагноз «рак кожи» имеет номер МКБ С44. МКБ – это международная статистическая классификация болезней и проблем, связанных со здоровьем. В данный момент применяется ее 10 версия (МКБ 10).
Ответы на все эти вопросы вы найдете в нашей статье, написанной простым и доступным языком.
Написано людьми для людей.
Теми, кто боролся, для тех, кому эта борьба предстоит.
Для оценки прогноза заболевания и выбора подходящего лечения применяется стадирование по системе AJCC (American Joint Committee on Cancer — Американского объединенного комитета по изучению рака).
Характеристики роста опухоли закодированы тремя буквами: T, N и M. Каждая из них (размер опухоли, количество пораженных лимфоузлов, наличие или отсутствие метастазов) влияет на прогноз течения заболевания и схему лечения.
Размеры опухоли: T = Tumor, опухоль
Буквой Т в сочетании с цифрами и буквами врачи обозначают наличие или отсутствие первичной опухоли, ее размер, количество пораженных тканей и органов:
Tx — недостаточно данных для оценки первичных данных (необходимо дополнительное обследование).
Т0 — первичная опухоль неизвестна (например, если метастазы найдены, а первичная опухоль — нет).
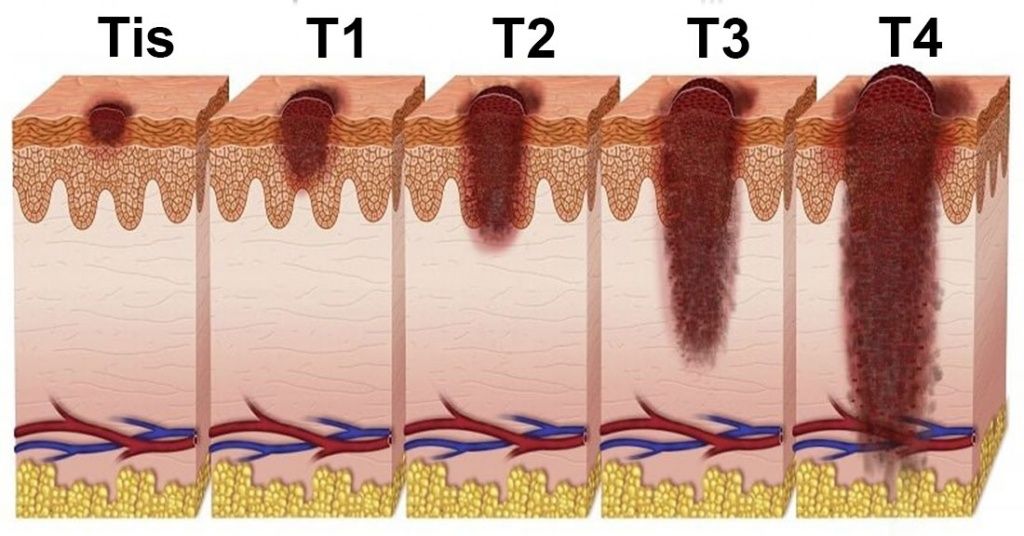
Tis — так называемая «карцинома in situ» — это аномальные клетки, отличающиеся от здоровых, которые растут и размножаются в верхнем слое кожи. Это поверхностная форма рака, то есть внутренние ткани не повреждены.
Т1 — опухоль размером не более 2 см.
T2 — опухоль размером от 2 до 4 см.
T3 предполагает несколько вариантов размеров и прорастания опухоли:
—опухоль больше 4 см;
—либо опухоль незначительно повредила кость, над которой находится участок пораженной раком кожи;
—либо опухоль проросла в окружающее нерв пространство (так называемая «периневральная инвазия»);
—либо глубокое поражение тканей.
T4 — опухоль глубоко проросла в кость или в костный мозг:
T4a — опухоль глубоко проросла в кортикальный слой кости (Кортикальный слой — это самая прочная оболочка костной ткани) или в костный мозг;
T4b — опухоль поразила череп или позвоночник.
Буква Т без цифровых уточнений информации о размере опухоли не содержит.
Лимфатические узлы: N = Nodes, лимфоузлы
Лимфатические узлы (лимфоузлы) работают как фильтры, помогая бороться с инфекцией и удаляя вредные вещества из организма. В теле человека их сотни.
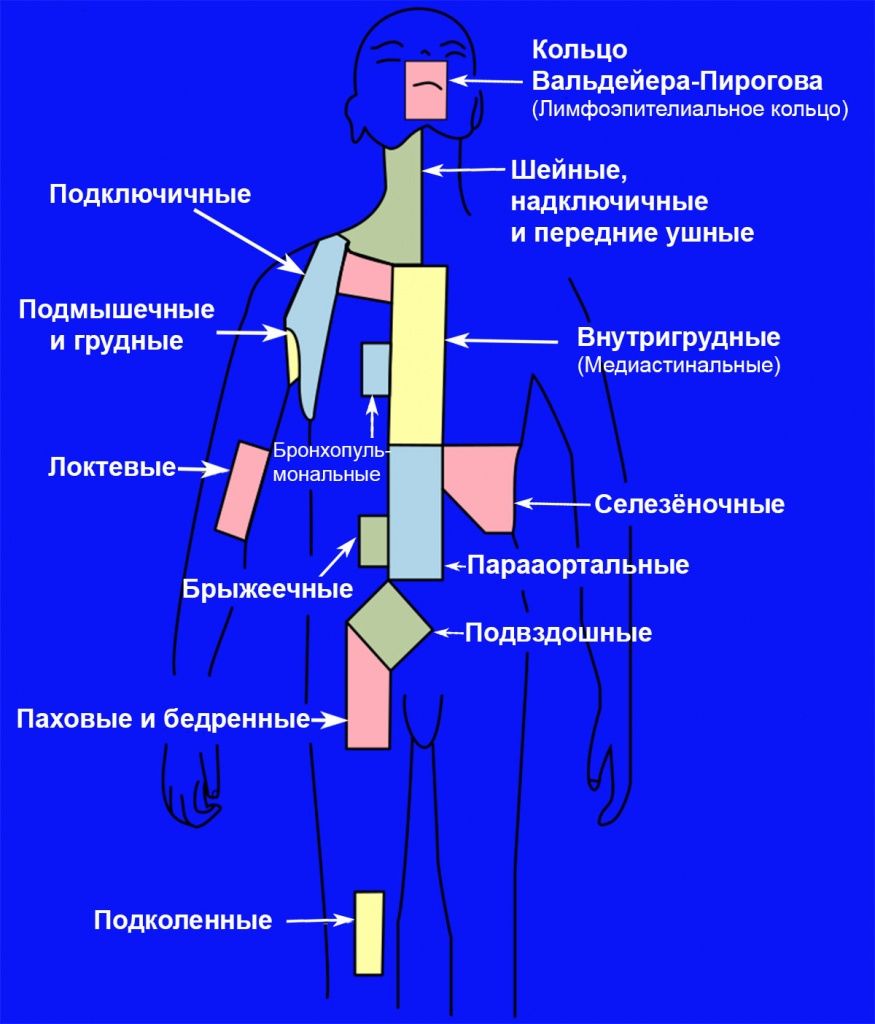
Регионарными называют лимфатические узлы определенного участка тела — например, шейные или надключичные.
Очень важно знать, поразил ли рак лимфоузлы — это значительно влияет на схему и тактику лечения.
Для описания количества и типа пораженных лимфоузлов врачи используют буквенное обозначение «N» в сочетании с цифрами:
NX означает, что для оценки состояния лимфоузлов недостаточно данных.
N0 — метастазов в регионарных лимфатических узлах нет.
N1 — метастаз в 1 лимфатическом узле на стороне поражения размером до 3 см.
N2 — метастаз в 1 лимфатическом узле размером более 3, но менее 6 см, либо несколько метастазов размером не больше 6 см каждый.
N3 — метастаз или метастазы более 6 см в одном или нескольких лимфатических узлах.
Буква «N» без цифровых обозначений информации о наличии/отсутствии пораженных лимфоузлов не содержит.
Если опухоль расположена на одной стороне тела (левой или правой), то регионарными лимфатическими узлами считаются:
Метастазы: M = Metastasis
Каждая здоровая клетка организма имеет свое определенное место в ткани или органе. Раковые клетки могут перемещаться по организму, создавая опухоль в разных частях тела.
Опухоль, созданная в результате деления этих клеток, называется метастазом.
Для описания наличия или отсутствия метастаз используется обозначение «M» в сочетании с цифрами или буквами:
M0 — метастазов в другие органы нет.
M1 — раковые клетки распространились в другие части организма и создали метастазы — вторичные опухоли. «М1» означает, что у вас 4 стадия рака кожи.
Без уточняющих цифр «M» не содержит информации о наличии или отсутствии метастазов.
Рак кожи стадируется на основе информации о T, N и M.
В стадиях дополнительно используются уточняющие буквенные обозначения. Важно понимать, что одинаковое обозначение стадии не означает одинаковую ситуацию. Например, 3 стадия может кодироваться как T3N0M0, T1N1M0, T2N1M0, T3N1M0. То есть при разных размерах опухоли, разном количестве пораженных лимфатических узлов будет указана одна стадия.
0 СТАДИЯ РАКА КОЖИ
Эта стадия называется «карцинома in situ». Кодируется как TisN0M0 и представляет из себя аномальные клетки, отличающиеся от здоровых, которые растут и размножаются в поверхностном слое кожи, превращаясь в опухоль. Это поверхностная форма рака, то есть внутренние ткани не повреждены, лимфатические узлы не поражены и метастазов Метастазы — это опухоли, образованные перемещающимися по организму раковыми клетками. Такие клетки попадают в другой орган, прикрепляются там и размножаются, создавая опухоль в другие органы нет.
1 СТАДИЯ РАКА КОЖИ
Кодируется как T1N0M0. На данной стадии развития заболевания опухоль имеет размеры 2 см или меньше, лимфатические узлы здоровы, и в других органах метастазов нет.
2 СТАДИЯ РАКА КОЖИ
Кодируется как T2N0M0. Это означает, что опухоль имеет размеры от 2 до 4 см (в любом измерении не превышает эти размеры), лимфатические узлы не поражены и метастазов Метастазы — это опухоли, образованные перемещающимися по организму раковыми клетками. Такие клетки попадают в другой орган, прикрепляются там и размножаются, создавая опухоль в другие органы нет.
3 СТАДИЯ РАКА КОЖИ
Классификация по ТНМ, кодируется как T3N0M0, T1N1M0, T2N1M0, T3N1M0. Этот набор шифров значит, что к данной стадии относят разные размеры поражения организма. Опухоль может иметь размеры от минимальных до значительных, включая прорастание в кость. Лимфоузлы могут быть здоровы или поражены, а вот метастазов на данной стадии нет. Чтобы понять, что именно с вами происходит, посмотрите свою медицинскую документацию. Расшифровки диагнозов:
4 СТАДИЯ РАКА КОЖИ
Классификация по ТНМ согласно клиническим рекомендациям. Кодируется как T1N2M0, T1N3M0, T2N2M0, T2N3M0, T3N2M0, T3N3M0, T4aNлюбаяM0, T4bNлюбаяM0TлюбаяNлюбаяM1.
Это единственная стадия, при которой в диагнозе будет указано «М1», а не «М0».
4 стадия не обязательно означает наличие метастазов, посмотрите свои медицинские документы и найдите там закодированный буквами T, N и M диагноз. Расшифровки диагнозов:
IVA стадия рака кожи (классификация по ТНМ) кодируется как T1N2M0, T1N3M0, T2N2M0, T2N3M0, T3N2M0, T3N3M0, T4aNлюбаяM0 (T4aN0M0, T4aN1M0, T4aN2M0, T4aN3M0), T4bNлюбаяM0 (T4bN0M0, T4bN1M0, T4bN2M0, T4bN3M0).
T4aNлюбаяM0 (T4aN0M0, T4aN1M0, T4aN2M0, T4aN3M0) означает, что:
T4bNлюбаяM0 (T4bN0M0, T4bN1M0, T4bN2M0, T4bN3M0) означает, что:
IVB стадия рака кожи (классификация по ТНМ) кодируется как TлюбаяNлюбаяM1(T1N0M1, T2N0M1, T3N0M1, T4aN0M1, T4bN0M1,T1N1M1, T2N1M1, T3N1M1, T4aN1M1, T4bN1M1, T1N2M1, T2N2M1, T3N2M1, T4aN2M1, T4bN2M1,T1N3M1, T2N3M1, T3N3M1, T4aN3M1, T4bN3M1).
Это означает, что после букв T и N может находиться любая цифра, означающая любое поражение. Важным отличием этой стадии от остальных является наличие метастазов — опухолей, возникших распространения раковых клеток по организму. Такие клетки перемещаются по органам и тканям с помощью лимфы Лимфа — это прозрачная жидкость, которая снабжает клетки водой и питательными веществами. Она содержит особые иммунные клетки, которые борются с инфекцией или крови, прикрепляются в любом месте и начинают расти и размножаться, создавая вторичную опухоль — метастаз.
(кроме раков кожи века, головы, шеи, перианальной области, вульвы и полового члена)
Рак кожи базальноклеточный и плоскоклеточный. Клинические рекомендации.
Рак кожи базальноклеточный и плоскоклеточный
Оглавление
Ключевые слова
Список сокращений
БКР – базальноклеточный рак
ПКР – плоскоклеточный рак кожи
Анти-CTLA4 – моноклональное антитело, блокирующее антиген цитотоксических Т-лимфоцитов 4 типа
Анти-PD1 – моноклональное антитело, блокирующее рецептор программируемой смерти 1
БСЛУ – биопсия сторожевого лимфатического узла
ВОЗ – всемирная организация здравоохранения
КТ – компьютерная томография
МКА – моноклональные антитела
МКБ-10 – международная классификация болезней, 10 пересмотр
МРТ магниторезонансная томография
ПЭТ позитронно-эмиссионная томография
ПЭТ-КТ позитронно-эмиссионная томография, совмещенная с компьютерной томографией
УЗДГ ультразвуковая допплерография
УЗИ ультразвуковое исследование
AJCC – American Joint Committee on Cancer
BRAF V600 – мутация в гене BRAF в 600 позиции 15 экзона с заменой нуклеотида, кодирующего валин на другую аминокислоту (чаще всего на нуклеотид, кодирующий глутаминовую кислоту V600E)
CTLA4 – антиген цитотоксических Т-лимфоцитов 4 типа (также известен как СD152) (выполняет функции рецептора, лигандом служит молекула B7.1 или B7.2)
ECOG – восточная кооперированая онкологическая группа
iBRAF – ингибитор мутантного белка BRAF (малая молекула, блокирующая тирознкиназу BRAF)
iMEK – ингибитор немутатного белка MEK (малая молекула, блокирующая тирознкиназу МЕК)
MEK – внутриклеточная сигнальная молекула (протеинкиназа, также известная как MAPK/ERK киназа)
PD-L1,2 – лиганд рецептора программируемой смерти 1 или 2
PD1 – рецептор программируемой смерти 1
UICC – Union International Contre Le Cancer (Union International for Cancer Control)
1. Краткая информация
1.1 Определение
1.2 Этиология и патогенез
Не существует единого этиологического фактора для развития немеланомных опухолей кожи. Самым значимым фактором риска спорадических (ненаследственных) форм немеланомных опухолей кожи следует считать воздействие на кожу ультрафиолетового излучения типа. При этом чувствительность кожи к ультрафиолетовому воздействию различается у людей и может быть классифицирована на 6 типов, где 1 и 2 отличаются наибольшей чувствительностью (и, соответственно, вероятностью возникновения солнечного ожога), а 5 и 6 – наименьшей [1, 2]. Также следует отметить такие факторы риска как врожденный или приобретенный иммунодефицит (например, после трансплантации органов или других заболеваниях, связанных с необходимостью принимать иммунносупрессанты), пигментная ксеродерма [2]. Описана связь между искусственным ультрафиолетом (в том числе PUVA-терапией) и повышением риска возникновения немеланомных опухолей кожи. Лица, имеющие контакт с мышьяком, также имеют повышенный риск возникновения ПКР, в частности болезни Боуэна [2]. В многих случаях немеланомные опухоли кожи развиваются на фоне предсуществующих предопухолевых новообразований (вроде актинического кератоза или кератоакантомы), которые также часто могут быть обнаружены на соседних со злокачественной опухолью участках кожи [2].
Существует также ряд наследственных синдромов, в рамках которых возможно возникновение базалиом: синдром невоидных базалиом (также известен как синдром Горлина-Гольтца), синдром Базекса, синдром Ромбо, синдром одностороннего базальноклеточного невуса [2].
При синдроме Горлина-Гольца обнаруживается мутация в гене PTCH, а у пациентов помимо множественных базалиом может быть выявлен характерный фенотип: широкий корень носа, дополнительные складки на ладонях, кистозные изменения челюстей, пороки развития костной системы. Синдром Базекса наследуется Х-сцепленно по доминатному принципу. Помимо развития множественных базалиом отмечается атрофодермия, гипотрихоз, гипогидроз, фолликуляная атрофия. Синдром Ромбо наследуется по аутосомнодоминантному принципу. По мимо множественных базалиом для синдрома Ромбо характерны гипертрихоз, вермикулярная атрофодермия, трихоэпителиомы и периферическая вазодилатация. При синдроме одностороннего базальноклеточного невуса у пациента отмечается врожденное новообразование кожи с комедонами и эпидермальными кистами, при микроскопии отмечается пролиферация базального эпителия [2].
1.3 Эпидемиология
1.4 Кодирование по МКБ-10
Другие злокачественные новообразования кожи (C44):
C44.1 – Рак кожи века, включая спайку век;
C44.2 – Рак кожи уха и наружного слухового прохода;
C44.3 – Рак кожи других и неуточненных частей лица;
C44.4 – Рак кожи волосистой части головы и шеи;
C44.5 – Рак кожи туловища (включая кожу перианальной области, кожу ануса и пограничную зону, кожу грудной железы;
C44.6 – Рак кожи верхней конечности, включая область плечевого сустава;
C44.7 – Рак кожи нижней конечности, включая область тазобедренного сустава;
C44.8 – Рак кожи, выходящий за пределы одной и более вышеуказанных локализаций;
C44.9 – Рак кожи неуточненный.
1.5 Классификация
1.5.1 Международная гистологическая классификация опухолей кожи ВОЗ 2006 [5]
I. Базальноклеточная карцинома 8090/3:
– узловая (солидная) 8091/3;
– с придатковой дифференцировкой 8098/3;
– базальноплоскоклеточная карцинома с ороговением 8090/3.
II. Плоскоклеточная карцинома 8070/3:
Морфологические типы не оказывают самостоятельного влияния на прогноз течения болезни, но осведомленность о различных клинических вариантах развития меланомы кожи может быть полезна на этапе осмотра для дифференциальной диагностики с доброкачественными новообразованиями кожи.
1.6 Стадирование
1.6.1 Стадирование меланомы кожи по системе UICC TNM (7 пересмотр, 2009 [6])
Для процедуры стадирования меланомы гистологическое подтверждение обязательно. Оценку состояния лимфатических узлов для установления стадии выполняют при помощи клинического осмотра и инструментальных исследований.
Критерий Т отражает распространенность первичной опухоли[*][7]:
Примечание: в случае первично-множественных синхронных опухолей классификация выполняется по опухоли наибольшего размера, а в скобках указывается общее количество опухолей кожи, например: T2 (5) [6].
Критерий N указывает на наличие или отсутствие метастазов в регионарных лимфатических узлах [6].
Регионарными лимфатическими узлами следует считать для опухолей, расположенных преимущественно на одной стороне тела (левой или правой):
В случае расположения опухоли в пограничных зонах лимфоузлы с обеих сторон могут считаться регионарными [6].
В таблице 1 приведены анатомические ориентиры для определения пограничных зон шириной 4 см.
Таблица 1. Анатомические ориентиры пограничных зон для определения регионарных лимфатических бассейнов
Линия границы (шириной 4 см)
Левая и правая половины
Срединная линия тела
Голова и шея / грудная стенка
Ключица – акромион – верхний край плеча
Грудная стенка / верхняя конечность
Грудная стенка / живот, поясница или ягодицы
Спереди: середина расстояния между пупком и реберной дугой;
Сзади: нижняя граница грудного позвонка (поперечный отросток)
Живот, поясница или ягодицы / нижняя конечность
Паховая складка – большой вертел – ягодичная борозда
При обнаружении метастазов в лимфатических узлах за пределами указанных регионарных зон метастазирования следует классифицировать их как отдаленные метастазы [6].
Критерий G характеризует степень дифференцировки опухоли [6]:
Некоторые факторы неблагоприятного прогноза суммированы в таблице 2. В классификации AJCC наличие таких факторов может повысить стадию с I до II [7].
Таблица 2. Факторы неблагоприятного прогноза рака кожи [6]
Глубина поражения/ инвазия микроструктур
Толщина опухоли более 4 мм по Бреслоу
Уровень инвазии по Кларку 4
Анатомическая локализация
Первичная локализация на ушной раковине
Первичная локализация на красной кайме губы
Дифференцировка
Низкодифференцированная или недифференцированная опухоль
Группировка по стадиям представлена в таблице 3:
Таблица 3. Группировка по стадиям немеланомных опухолей кожи [6]
Рак кожи
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «14» марта 2019 года
Протокол №58
Название протокола: Рак кожи
Коды по МКБ – 10:
| МКБ-10 Код | |
| Код | Название |
| С 44 | Другие злокачественные новообразования кожи |
| C44.0 | Кожи губы |
| C44.1 | Кожи века, включая спайку век |
| C44.2 | Кожи уха и наружного слухового прохода |
| C44.3 | Кожи других и неуточненных частей лица |
| C44.4 | Кожи волосистой части головы и шеи |
| C44.5 | Кожи туловища |
| C44.6 | Кожи верхней конечности, включая область плечевого пояса |
| C44.7 | Кожи нижней конечности, включая тазобедренную область |
| C44.8 | Поражения кожи, выходящие за пределы одной и более выше- |
| C44.9 | Злокачественные новообразования кожи неуточненной области |
Дата разработки/пересмотра протокола: 2015 г/2018 г
Пользователи протокола
Онкологи, хирурги, радиологи, химиотерапевты, стоматологи, нейрохирурги, лучевые диагносты, врачи общей практики, терапевты, врачи скорой и неотложной помощи, студенты мед ВУЗов, резиденты.
Категория пациентов: взрослые
Шкала уровня доказательности
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
· Плоскоклеточные опухоли
Внутриэпидермальный плоскоклеточный рак (canser in situ):
Болезнь Боуэна
Эритроплазия Кейра
Инфильтрирующий плоскоклеточный рак:
Акантолитический тип
Веретеноклеточный тип
Веррукозный тип (полости рта, аногенитальной области, подошвы, других участков)
псевдососудистая
аденоплоскоклеточная
· Базально-клеточные опухоли
Поверхностная (Мультицентрическая) базально-клеточная карцинома.
Солидная (узловая или нодулярная)
Микроузловая (микронодулярная)
нфильтративная (инфильтрирующая): склеродермоподобная, несклерозирующийся тип.
Фиброэпителиальная (фиброэпителиома Пинкуса)
Базальноклеточная карцинома с дифференцировкой в сторону придатков кожи
Пигментная
Базальноклеточная карцинома со смешанным типом роста
· Опухоли придатков кожи
Аденокарцинома апокринная.
Рак сальных желез.
Рак потовых желез
трихолеммокарцинома
· Другие опухоли
Недифференцированная карцинома, БДУ.
Болезнь Педжета, экстрамаммарная.
Карцинома кожи (исключая веки, голову и шею, перианала, вульвы и пениса)
(ICD-O-3 C44,5-7, C63,2)
Классификация применяется только к карциномам, за исключением карциномы клеток Меркель. Там должно быть гистологическое подтверждение заболевания и деление случаев гистологическим тип.
примечание
* Глубокое поражение определяется как поражение за пределы подкожного жира или> 6 мм (измеряется от гранулированного слоя соседнего нормального эпидермиса до основания опухоли); периневральная инвазия для классификации Т3 определяется как клинически или рентгенографически вовлечение нервов без вовлечения основания черепа или с поражением основания или нарушение функции.
В случае первично-множественных опухолях с самой высокой категорией Т и количество отдельных опухолей указано в скобках, например, T2 (5).
Патологическая классификация pTNM
Категории pT и pN соответствуют категориям T и N.
pN0. Гистологическое исследование удаленного регионального лимфоузла обычно
включают 6 или более лимфатических узлов. Если лимфатические узлы отрицательные, но число обычно проверяется, не классифицируется как pN0.
Стадии
Стадия 0 Tis N0 M0
Стадия I T1 N0 M0
Стадия II T2 N0 M0
Стадия III T3 N0 M0
T1, T2, T3 N1 M0
Стадия IVA T1, T2, T3 N2, N3 M0
T4 N любая M0
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез
Базальноклеточный рак кожи:
Поверхностная форма начинается с появления ограниченного шелушащегося пятна розовой окраски. Затем пятно приобретает четкие контуры, по краю очага появляются плотные мелкие поблескивающие узелки, которые сливаются между собой и образуют приподнятый над уровнем кожи валикообразный край. Очаги поражения могут быть солитарными или множественными. Среди поверхностных форм выделяют саморубцующуюся или педжетоидную базалиому.
При пигментной форме базалиомы цвет очага поражения имеет диффузную, чаще неравномерную пигментацию бурой или черно-коричневой окраски с наличием полупрозрачных, «перламутровых» участков и поверхностных телеангиэктазий. Пигментная форма в виде узла или бляшки может напоминать приобретенные сложные или внутридермальные меланоцитарные невусы. Узловая меланома клинически также может напоминать базалиому, но последняя имеет более плотную консистенцию. Изъязвившаяся пигментная базалиома может легко прията клиницистом за меланому. При этом необходимо учитывать, базалиома располагается преимущественно на лице, меланома на любых участках кожного покрова. Правильной диагностике помогают мерфологические методы исследования.
Опухолевая форма базалиомы характеризуется возникновением узелка, который постепенно увеличивается в размерах. Поверхность опухоли гладкая с выраженными телеангиэктазиями, иногда покрыта сероватыми чешуйками. Иногда центральная часть ее изъязвляется и покрывается плотными корками. В зависимости от величины различают мелко- и крупноузелковую формы базалиомы.
Характерным признаком язвенной формы является воронкообразное изъязвление и массивный, спаянный с подлежащими тканями инфильтрат с нечеткими границами, которые по размерам больше самой язвы.
Склеродермоподобная, или рубцово-атрофическая, форма представляет собой небольшой, четко отграниченный очаг поражения. Характерно инфильтрирующий рост и развитие соединительнотканной стромы. Растет медленно. Очаг выглядит как белесый склерозированный участок с «перламутровыми» папулами по периферии, в центре – телеангиэктазии.
Фиброэпителиальную опухоль Пинкуса относят к разновидности базалиом, хотя ее течение более благоприятное. Клинически она проявляется в виде узелка или бляшки цвета кожи, плотноэластической консистенции, практически не подвергается эрозии. Может напоминать большой кожный выступ или фиброму. Растет медленно. Локализуется преимущественно в нижней части спины или живота.
Плоскоклеточный рак кожи:
Поверхностная форма — наиболее частый вариант рака кожи. Она начинается с одного или нескольких сливающихся безболезненных узелков величиной чуть больше спичечной головки. Узелок слегка возвышается над поверхностью кожи, имеет желтоватый или матово-белый цвет и плотную консистенцию. С течением времени опухоль увеличивается в размерах и приобретает вид безболезненной бляшки желтого или серовато-белого цвета с восковидным оттенком, слегка возвышающейся над кожей. Поверхность ее гладкая или шероховатая. Края выступают в виде плотного валика с неровным фестончатым контуром. В дальнейшем в центре бляшки появляется западение, покрытое чешуйкой или корочкой. Удаление корочки приводит к появлению капельки крови. С увеличением размеров опухоли западение превращается в эрозированную поверхность, покрытую коркой и окруженную плотными неровными краями в виде круто выступающего, как бы срезанного валика.
Инфильтрирующая форма имеет вид глубоко изъязвления с неровным, бугристым, покрытым корками из некротических масс дном и плотными, валикообразными краями. Опухоль быстро прорастает окружающие ткани и становится неподвижной. Такое новообразование по гистологической структуре обычно является плоскоклеточным раком. Папиллярная форма рака кожи встречается редко. Она имеет вид плотного, возвышающегося над поверхностью, легко кровоточащего узла на широком основании. Поверхность узла бугриста, покрыта корками, часто напоминает цветную капусту.
Метатипический рак обычно представляет собой язвенный опухолевый очаг, в 95% случаев размером 1-3 см в диаметре. Язвенный дефект неправильной формы с неровными обрывистыми или подрытыми краями. Дно язвы неровное, имеет ярко-розовую поверхность с некротическими массами.
Физикальное обследование включает тщательный осмотр кожи от волосистой части головы до пяток и периферических лимфатических узлов, оценка состояния внутренних органов.
Лабораторные исследования (напр.: повышение уровня лейкоцитов в крови с указанием цифровых показателей нормы и/или показателей патологического состояния):
• ОАМ;
• ОАК;
• Биохимический анализ крови (билирубин, общий белок, АЛТ, АСТ, мочевина, креатинин, глюкоза, ЛДГ);
• Коагулограмма (протромбин, протромбиновый индекс, протромбиновое время, нормализованное отношение (МНО), фибриноген, антитромбин III, активированное парциальное (частичное) тромбопластиновое время (АПТВ/АЧТВ)
• Реакция микропреципитации
• Определение антигена p24 ВИЧ в сыворотке крови ИФА-методом
• Определение HBsAg, гепатит С в сыворотке крови ИФА-методом
• ЭКГ
• Пациенты старше 50 лет – консультация кардиолога.
Инструментальные исследования (рентгенологические признаки, ЭГДС – картина):
• Взятие соскоба с поверхности эрозий, изъязвлений кожи, пунктатов уплотнений кожи без признаков изъязвлений и увеличенных л/у для цитологического исследования. При неясности цитологического исследования необходима биопсия для гистологического подтверждения диагноза.
• рентгенография органов грудной клетки.
• УЗИ периферических лимфоузлов
• УЗИ органов брюшной полости и забрюшинного пространства
• КТ костей в случае подозрения распространения опухоли в кость
• ТАБ под контролем УЗИ при подозрении на метастазы в регионарные л/у
• при подготовке к хирургическому лечению с целью оценки функционального статуса по показаниям проводить дополнительное обследование: эхокардиографию, исследование функции внешнего дыхания, УЗДГ сосудов шеи и нижних конечностей
Показания для консультации специалистов (напр.: онколога с указанием цели консультации):
• консультация кардиолога (пациентам 50 лет и старше, так же пациенты моложе 50 лет при наличии сопутствующей патологии сердечно-сосудистой системы);
• консультация невропатолога (при сосудистых мозговых нарушениях, в том числе инсультах, травмах головного и спинного мозга, эпилепсии, миастении, нейроинфекционных заболеваниях, а также во всех случаях потери сознания);
• консультация гастроэнтеролога (при наличии сопутствующей патологии органов ЖКТ в анамнезе);
• консультация нейрохирурга (при наличии метастазов в головной мозг, позвоночник);
• консультация торакального хирурга (при наличии метастазов в легких);
• консультация эндокринолога (при наличии сопутствующей патологии эндокринных органов).
Диагностический алгоритм: (схема)
Пациент → первичный клинический осмотр кожных покровов → терапевт, профильный специалист → обследование, верификация диагноза:
— выявление и формирование групп повышенного риска – активное наблюдение у профильного специалиста/ терапевта
— ЗНО, подозрение на ЗНО – лечение в ООД по месту жительства, КазНИИОиР- наблюдение онколога по месту жительства
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Дифференциальную диагностику проводят в зависимости от типа опухоли кожи
| Диагноз | Обоснование для дифференциальной диагностики | Обследования | Критерии исключения диагноза |
| Болезнь Боуэна | Может быть крупной бляшкой как и поверхностная форма базалиомы | Локальный осмотр Цитологическое и гистологическое исследование | Бляшка плоская с неровными очертаниями и без узелков в краевой зоне. Чаще локализуется на туловище, верхних конечностях и в промежности. Диагноз устанавливается после гистологического исследования |
| Кератоакантома | купол с небольшой лункой в центре. Края у лунки четкие, в центре имеется кратерообразное углубление «псевдоязва», в центре заполненное плотными или рыхлыми массами серо-коричневого цвета, не кровоточит Оттенок узелка обычно красноватый, серый или синеватый, иногда новообразование имеет цвет кожи. | Локальный осмотр Цитологическое и гистологическое исследование | Гистологически отличить от рака бывает сложно Быстрый рост Наличие фазы стабилизации Роговые массы безболезненны, не кровоточит |
| Склеродермия | Ограниченная форма схожа со склеродермоподобной базалиомой | Локальный осмотр | Плотные бляшки более крупные восковидной или розовато-лиловой окраски с правильными очертаниями и зоной застойной эритемы по периферии. |
| Красная волчанка | При наличии единственного очага поражения внешне напоминает поверхностную форму базалиомы | Локальный осмотр | Редко продолжительное время имеет только один очаг, имеется периферическая зона эритемы и фолликулярный гиперкератоз |
| Сложные, внутридермальные невусы | Если базалиома пигментная размером до 1см. | Локальный осмотр дерматоскопия | Появляюся в пубертантном периоде или юности |
| Узловая меланома | Изъязвившаяся пигментная форма базалиомы легко принимается за меланому | Располагаются на любых участках кожного покрова. Диагноз устанавливается после гистологического исследования | |
| Доброкачественная лимфоплазия кожи | Как и нодулярная базалиома округлой формы, располагается на лице. | Имеет тестоватую консистенцию и синюшно-розовую окраску с буроватым отттенком. | |
| Дерматофиброма | Как нодулярная базалиома может иметь большие размеры более 3см, гладкую бугристую поверхность, с течением времени изъязвляться медленно расти | Локальный осмотр Цитологическое и гистологическое исследование | Необходимо гистологическое исследование |
| Плоскоклеточный рак | С язвенной формой базалиомы, которая имеет инвазивно-деструктивный рост в подлежащие ткани и кости | Величина язвы соответствует границам опухоли, отделяемое со зловонным запахом, могут возникать метастазы. |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Апрепитант (Aprepitant) |
| Блеомицин (Bleomycin) |
| Висмодегиб (Vismodegib) |
| Гранисетрон (Granisetron) |
| Дексаметазон (Dexamethasone) |
| Доксорубицин (Doxorubicin) |
| Метоклопрамид (Metoclopramide) |
| Метотрексат (Methotrexate) |
| Нетупитант (Netupitant) |
| Оланзапин (Olanzapine) |
| Ондансетрон (Ondansetron) |
| Палоносетрон (Palonosetron) |
| Ролапитант (rolapitant) |
| Трописетрон (Tropisetron) |
| Фосапрепитант (Fosaprepitant) |
| Цисплатин (Cisplatin) |
| Этопозид (Etoposide) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Немедикаментозное лечение (режим, диета и пр. лучевое); Режим общий, стол 15
Медикаментозное лечение
Хирургическое вмешательство на амбулаторном уровне
— хирургические лечение – иссечение опухоли кожи под местной анестезией с гистологическим исследованием
— криотерапия
— лучевая терапия по радикальной программе (разовая суммарная доза подбирается с учетом локализации, размера опухоли, глубины поражения и цитологической или морфологической верификации опухоли). Близкофокусная рентгенотерапия. Дистанционная лучевая терапия на линейных ускорителях.
Дальнейшее ведение
После хирургического лечения: ежедневно перевязки, антибиотикотерапия
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВН Е
Карта наблюдения пациента, маршрутизация пациента (схемы, алгоритмы)
Пациент → первичный клинический осмотр кожных покровов → терапевт, профильный специалист → обследование, верификация диагноза → ЗНО, подозрение на ЗНО – лечение в ООД по месту жительства или КазНИИОиР.
Режим больного при проведении консервативного лечения – общий. В раннем послеоперационном периоде – постельный или полупостельный (в зависимости от объема операции и сопутствующей патологии). В послеоперационном периоде – палатный.
Лимфодиссекция выполняется при наличии метастазов в лимфатических узлах и производится одновременно с удалением первичного опухолевого очага или при выявлении.
Профилактическая лимфодиссекция не выполняется.
Стандартными хирургическими вмешательствами на лимфатическом аппарате являются: подключично-подмышечно-подлопаточная, подвздошно-пахово-бедренная, классическая радикальная шейная (операция Крайла), модифицированная радикальная шейная лимфодиссекция III типа (футлярно-фасциальная шейная). Пахово-бедренная лимфодиссекция. Операция Дюкена.
Лечение по стадиям
I и II стадии (T1-2N0M0):
В случае выявления при плановом гистологическом исследовании положительные края резекции показана адъювантная ЛТ или реиссечение.
Или лучевая терапия по радикальной программе (разовая суммарная доза подбирается с учетом локализации, размера опухоли, глубины поражения и цитологической или морфологической верификации опухоли). Близкофокусная рентгенотерапия. Дистанционная лучевая терапия на линейных ускорителях.
IV стадия (любая Т любая N M1):
лечение паллиативное или симптоматическое по индивидуальным программам после обсуждения на МДГ (могут использоваться хирургические методы, лучевая терапия, системная химиотерапия, электрохимиотерапия).
Плоскоклеточный рак, метатипический рак, рак придатков кожи:
I стадия :
В случае выявления при плановом гистологическом исследовании положительные края резекции показана адъювантная ЛТ.
III стадия (любая T N1 M0):
IV стадия (любая Т любая N M1):
лечение паллиативное или симптоматическое по индивидуальным программам после обсуждения на МДГ (могут использоваться хирургические методы, лучевая терапия, системная химиотерапия, электрохимиотерапия).
Томотерапия на томоаппаратах. Одним из вариантов высокотехнологичной лучевой терапии РТМ является Томотерапия – спиральное (гелическое “helical”) облучение, проводимое на специализированных линейных ускорителях – томоаппаратах. При их работе происходит одновременное ротационное движение во время сеанса облучения головки аппарата и лепестков (секторное IMRT) с одновременным поступательным продольным смещением стола. Спиральная томотерапия это сверхточная лучевая терапия управляемая по изображениям (IGRT), с помощью, которой осуществляется прецизионное подведение луча вращающего радиационного пучка к опухоли с одновременной защитой окружающих здоровых тканей, за счет визуализации и локализации анатомическихструктур на протяжении процесса лечения.Используемые в каждом направлении модулированные не только сверхточно фокусируется, но и характеризуется высокой конформностью. Существует много систем, которые позволяют создать сферическое распределение мелких доз, но томотерапия, позволяет изменить форму этой дозы при несферических и даже весьма сложных, вогнутых мишенях. Используются как стандартные методики фракционирования при подведении разовых и суммарных очаговых доз. Однако упор при томотерапии делается на гипофракционирование при РОД Схемы лекарственной терапии генерализованных форм рака кожи:
В) Цисплатин – 25мг/м2 в/в 1-5й дни
Метотрексат – 15мг/м2 в/в 1,8,15й дни
Блеомицин – 15мг в/в 1,3,5,8,10,12й дни
С) Этопозид – 100мг/м2 в/в 1-3й дни
Цисплатин – 100мг/м2 в/в 1й день
| Химиопрепараты | |
| Цисплатин-ЛЭНС | 50мг 2-3фл |
| Доксолек | 10мг, 50мг 5-10фл |
| Метотрексат | 10мг, 15мг, 50мг, 500мг, 1000мг |
| Блеомицин | 30мг |
| Этопозид | 100мг |
| Висмодегиб (только при базально-клеточном раке) | 150мг |
Сопроводительная терапия с целью профилактики и лечения побочных эффектов лекарственной терапии представлено в приложении 1.
Профилактика
Профилактика рака кожи заключается, прежде всего, в своевременном выявлении и активном лечении предраковых заболеваний, что требует онкологической настороженности у дерматологов и терапевтов.
При выявлении трансформации предракового дерматоза в рак дерматолог должен направить больного к онкологу, который будет решать вопрос о выборе тактики лечения.
Важная роль принадлежит санитарной пропаганде знаний среди населения о клинических проявлениях новообразования с тем, чтобы больные обращались к врачу в максимально ранние сроки при его возникновении.
Необходимо предупреждение населения о вредных последствиях инсоляции, особенно это касается блондинов со светлой кожей. О недопустимости воздействия УФИ должны быть предупреждены и больные ЗН кожи.
Нужно свести к минимуму применение лучевой терапии по поводу различных заболеваний кожи, в том числе базалиом, особенно у молодых лиц.
Важную роль в профилактике рака кожи играет соблюдение техники безопасности на производстве, где имеются канцерогенные вещества. Лица, занятые на таких производствах, должны подвергаться систематическим медосмотрам. связи с частой ассоциацией ВПЧ16 и ВПЧ18 с плоскоклеточным раком половых органов, для профилактики генитального рака целесообразно проведение вирусологического обследования на наличие групп риска.
Так как одним из важнейших факторов возникновения карциномы является хроническое повреждение солнечными лучами, прежде всего следует уделить внимание защите от солнца. Важнейшие правила:
— при пребывании на свежем воздухе следует по возможности находиться в тени,
— особенно в солнечные дни следует носить непроницаемую для солнечных лучей одежду, в том числе шляпу с по возможности широкими полями, а также использовать солнцезащитные кремы,
— солнечное излучение наиболее сильно в обед, между 10 и 15 часами. Солнечные ванны в это время наиболее вредны,
— лучевое повреждение могут оказывать также и искусственные ультрафиолетовые лучи (солярии, сварочные работы, УФ-терапия по медицинским показаниям).
Эти правила особенно важны для детей. Кожа у них особенно чувствительна, и дети обычно не могут самостоятельно контролировать свое пребывание под открытым небом.
Также очень важны регулярные контроли у врача-дерматолога, особенно для пожилых людей и людей из групп риска (например, после трансплантации органов), а также для тех, у кого уже были раковые заболевания кожи либо предстадии. Это делает возможным распознание в ранних стадиях, облегчает лечение и улучшает прогноз.
У тех, у кого однажды была базальноклеточная карцинома, существенно повышен риск повторного возникновения новой опухоли. Повторное заболевание развивается примерно у каждого третьего пациента, причём в большинстве случаев новые опухоли образуются в течение ближайших трёх лет. Поэтому ежегодные врачебные контроли в виде клинического осмотра кожи рекомендуются как минимум в течение трёх лет после окончания лечения. Кроме того, пациентам рекомендуется самим внимательно следить за своей кожей и в подозрительных случаях обращаться к врачу.
Программа активного диспансерного наблюдения за больными БКР в условиях ПМСП
Выявленные больные после проведенного лечения находятся по поводу БКР под активным диспансерным наблюдением (ДО-11) с целью раннего выявления рецидива и возможного лечения.
Целесообразно наблюдать больных без отягощающих факторов риска не болеем 3 лет. Этого срока наблюдения вполне достаточно для уточнения прогноза и выявления возможного рецидива заболевания. При этом осмотр проводится в первые 2года 4 раза в год, в 3- 1р в год.
Больных с первично-множественным рецидивирующим раком рекомендуется брать на активное наблюдение сразу пожизненно. Это обусловлено тем, что у больных первично-множественными формами заболевания число рецидивов в месте лечения опухоли было в 7,8 раза выше, чем у больных с единичной опухолью. Рецидивы в месте удаления рака у больных с единичной формой заболевания возникали на протяжении первых 3 лет наблюдения, а с множественной – на 3-5-м годах. В этой группе больных проводится углубленная ежегодная диспансеризация, направленная на раннее выявление онкологических заболеваний различной локализации.
Пациенты, получившие лечение по поводу плоскоклеточного, метатипического рака и придатков кожи рекомендуется проводить реабилитацию, ориентируясь на общие принципы реабилитации пациентов после проведенных хирургических вмешательств и/или химиотерапии.
ИНДИКАТОРЫ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ И БЕЗОПАСНОСТИ МЕТОДОВ ДИАГНОСТИКИ И ЛЕЧЕНИЯ, ОПИСАННЫХ В ПРОТОКОЛЕ
• Объективные признаки отсутствия опухоли, регрессии опухоли, мтс
• УЗИ данные об отсутствии мтс и рецидива
• Рентген данные об отсутствии отдаленных мтс
• Удовлетворительные показатели крови, мочи, биохимии
• Заживление послеоперационной раны
• Относительно удовлетворительное состояние больного (-ой)
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
Наличие на поверхности кожи единичного или множественных болезненных или безболезненных опухолевидных образований, шероховатых бляшек или кратерообразных язвенных дефектов, кровоточивость при контакте, увеличение периферических лимфоузлов, локальные боли
Показания для экстренной госпитализации:
• показаний для экстренной госпитализации для данного заболевания нет
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Указание на отсутствие конфликта интересов:
Конфликт интересов отсутствует.
Рецензенты:
1) Савхатов Доспул Хайназарович – доктор медицинских наук, доцент кафедры онкологии АО «Национальный медицинский университет»;
2) Тлеугабилова Гульнара Акынгалиева – кандидат медицинских наук, доцент кафедры онкология с курсом гематологии АО «Казахский медицинский университет непрерывного образования».
Указание условий пересмотра протокола: пересмотр протокола через 5 лет и/или при появлении новых методов диагностики/ лечения с более высоким уровнем доказательности.
Приложение 1
СОПРОВОДИТЕЛЬНАЯ ТЕРАПИЯ
Антиэметическая терапия
Тошнота и рвота являются одним из наиболее частых побочных эффектов химио- терапии (ХТ) и существенно ухудшают качество жизни больных.
Тошнота и рвота, сопутствующие химиотерапии, относятся к числу наиболее неприятных аспектов этого вида лечения (1,2). Не будучи самым серьезным побочным эффектом химиотерапии, рвота, тем не менее, сильно ухудшает качество жизни и снижает ощущение благополучия (1,3). В некоторых случаях пациенты откладывают или полностью прекращают химиотерапию из-за непереносимой тошноты и рвоты (1).
Кроме того, рвота, как таковая, может представлять угрозу здоровью, поскольку неконтролируемая рвота приводит к обезвоживанию, нарушению баланса метаболитов и к анорексии (4,5).
Факторы, связанные с терапией:
Высокая эметогенная способность некоторых препаратов,
Комбинированная терапия
Режим и способ введения препаратов
Высокие дозы химиотерапевтических препаратов (6).
Под уровнем эметогенности понимается риск развития рвоты у больных, получающих тот или иной цитостатик в монорежиме без противорвотной терапии. Например, высокий уровень эметогенности означает, что после введения препарата рвота будет развиваться более чем у 90 % больных. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO представлена в табл. 1.
Таблица 1. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO.
ТИПЫ ТОШНОТЫ И РВОТЫ
По срокам и механизму развития выделяют 3 основных типа тошноты и рвоты, вызванной цитостатиками: острую, отсроченную и условно-рефлекторную (anticipatory – переводят также как «предшествующую», «преждевременную», «рвоту ожидания»), дополнительно выделяют неконтролируемую (breakthrough – «прорывную») и рефрактерную (7, 8).
Острая рвота развивается в первые 24 ч после химиотерапии, отличается высокой интенсивностью, редко сопровождается тошнотой.
Отсроченная рвота развивается на 2-е–5-е сутки после начала химиотерапии, менее интенсивна, чем острая, и, как правило, сопровождается постоянной тошнотой. Механизмы развития остаются неясными. Ведущая роль отводится субстанции P, серотонин имеет меньшее значение.
Условно-рефлекторная рвота представляет собой классический условный рефлекс на химиотерапию и / или сопутствующие ей манипуляции и окружающую обстановку. Формируется в тех случаях, когда противоопухолевая терапия сопровождается тошнотой и рвотой. Риск ее развития увеличивается пропорционально числу проведенных курсов и может сохраняться в течение длительного времени после окончания химиотерапии. Ведущую роль в формировании условного рефлекса играет многодневная умеренная или тяжелая тошнота. Лучшим методом профилактики условно-рефлекторной тошноты и рвоты является адекватная антиэметическая защита пациента уже с первого курса химиотерапии.
Неконтролируемая (breakthrough – «прорывная») тошнота и рвота развивается на фоне адекватной антиэметической профилактики и требует дополнительной коррекции. Рефрактерная рвота возникает на последующих циклах химиотерапии при неэффективности противорвотной профилактики и / или препаратов резерва на предыдущих курсах лечения.
ПРИНЦИПЫ СОВРЕМЕННОЙ ПРОТИВОРВОТНОЙ ТЕРАПИИ
1. Обязательность проведения, начиная с первого курса химиотерапии.
2. Введение антиэметиков до начала введения первого цитостатика.
3. Применение наиболее эффективных стандартных противорвотных комбинаций.
4. Применение каждого антиэметика, входящего в комбинацию, в адекватных дозах.
5. Соблюдение адекватной продолжительности противорвотной терапии.
6. Соблюдение необходимых для сохранения эффективной концентрации интервалов между приемами антиэметиков.
Критерием эффективности противорвотной терапии является полное отсутствие (полный контроль) рвоты и тошноты в течение 24 часов (период развития острой рвоты) с момента введения противоопухолевых препаратов.
Алгоритм профилактики и терапии тошноты и рвоты
1. Определить эметогенный потенциал назначенного режима ХТ.
2. Назначить профилактическую терапию, исходя из эметогенности режима ХТ.
3. Назначить лечение в случае развития тошноты и рвоты на фоне профилактической терапии.
4. Внести изменения в профилактическую терапию тошноты / рвоты на последующих циклах ХТ.
Таблица 2. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Острая тошнота и рвота.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | 5-НТ3 + DEX + NK 1 |
| Высокий (АС) | 5-НТ3 + DEX + NK 1 |
| Карбоплатин | 5-НТ3 + DEX + NK 1 |
| Умеренный (кроме карбоплатина) | 5-НТ3 + DEX |
| Низкий | 5-НТ3 или DEX или DOP |
| Минимальный | Нет рутинной профилактики |
Таблица 3. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Отсроченная тошнота и рвота.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | DEX или (если APR 125мг для острой: (МСР+DEX) или (DEX+APR) |
| Высокий (АС) | Нет или (если APR 125мг для острой: APR+DEX) |
| Карбоплатин | Нет или (если APR 125мг для острой: APR) |
| Средний (не карбоплатин) | DEX можно использовать |
| Низкий | Профилактика не предусмотрена |
| Минимальный | Профилактика не предусмотрена |
Ключевые обновления в рекомендациях по контролю ТРВХ, NCCN 2017:
Карбоплатин категоризируется как высокоэметогенный препарат при введении с площадью под кривой (ППК) ≥4, при введении с ППК
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | 5-НТ3 + DEX* + NK 1+Olanzapine* |
| Высокий (АС) | 5-НТ3 + DEX* + NK 1+Olanzapine* |
| Карбоплатин | 5-НТ3 + DEX + NK 1 |
| Умеренный (кроме карбоплатина) | 5-НТ3 + DEX |
| Низкий | 5-НТ3 или DEX или DOP |
| Минимальный | Нет рутинной профилактики |
Таблица 5. Рекомендуемые дозы антогонистов серотониновых рецепторов (5-НТ) для острой тошноты и рвоты.