код заболевания g37 9
Демиелинизирующая болезнь центральной нервной системы неуточненная
Рубрика МКБ-10: G37.9
Содержание
Определение и общие сведения [ править ]
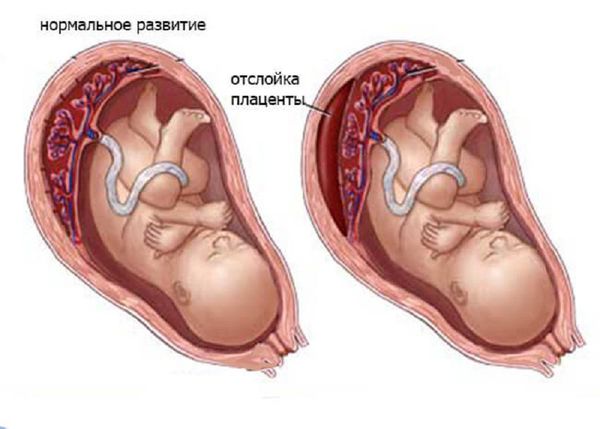
Острый рассеянный энцефаломиелит — сравнительно редкое нерецидивирующее демиелинизирующее заболевание головного и спинного мозга. Патоморфологически он характеризуется распространенной демиелинизацией и периваскулярной лимфоцитарной инфильтрацией и напоминает экспериментальный аллергический энцефаломиелит. Чаще всего он возникает при кори, ветряной оспе, краснухе через 4—6 сут после появления сыпи (постинфекционный энцефаломиелит) или на 10—15-й день после вакцинации против оспы или бешенства (поствакцинальный энцефаломиелит). Острый рассеянный энцефаломиелит у детей дифференцируют с синдромом Рейе (недемиелинизирующая постинфекционная энцефалопатия).
Этиология и патогенез [ править ]
Клинические проявления [ править ]
Демиелинизирующая болезнь центральной нервной системы неуточненная: Диагностика [ править ]
В легких случаях наблюдаются только головная боль, ригидность затылочных мышц, лихорадка и спутанность сознания. В тяжелых случаях могут возникать эпилептические припадки, тетраплегия, мозжечковая атаксия, множественные поражения черепных нервов, нарушения чувствительности и кома. На МРТ выявляется распространенное поражение белого вещества. В СМЖ обнаруживаются изменения, свойственные асептическому менингиту.
Дифференциальный диагноз [ править ]
Демиелинизирующая болезнь центральной нервной системы неуточненная: Лечение [ править ]
В неконтролируемых исследованиях показано, что кортикостероиды уменьшают тяжесть заболевания. Рекомендуют метилпреднизолон в той же дозе, что и при обострении рассеянного склероза. Одна из схем предусматривает метилпреднизолон в/в по 500 мг каждые 12 ч в течение 3 сут с последующим переходом на преднизон внутрь в дозе 60—80 мг/сут в течение 7 сут; затем дозу преднизона снижают каждую неделю на 20 мг. При эпилептических припадках показаны противосудорожные средства, при отеке мозга — маннитол. Необходима интенсивная поддерживающая терапия, поскольку у многих происходит полное или почти полное восстановление.
Профилактика [ править ]
Прочее [ править ]
Прогноз. Смертность при коревом энцефаломиелите составляет 10—20%, при поствакцинальных энцефаломиелитах — 30—50%. Примерно у 25—50% выживших остается грубый неврологический дефект.
Источники (ссылки) [ править ]
Дополнительная литература (рекомендуемая) [ править ]
1. Alvord, E. C. Acute Disseminated Encephalomyelitis and «Allergic» Neuroencephalopathies. In: P. J. Vinken and G. W. Bruyn (eds.), Handbook of Clinical Neurology. Amsterdam: North-Holland, 1970. Vol. 9, pp. 500—571.
2. Johnson, R. T., Griffin, D. E., and Gendelman, H. E. Post-infectious encephalomyelitis. Semin. Neurol. 5:180, 1985.
3. Kesselring, J., et al. Acute disseminated encephalomyelitis: MRI findings and the distinction from multiple sclerosis. Brain 113:291, 1990.
4. Pasternak, J. F., deVivo, D. C., and Prensky, A. L. Steroid-responsive encephalomyelitis in childhood. Neurology (Minneapolis) 30:481, 1980.
5. Scott, T. F. Post-infectious and vaccinial encephalitis. Med. Clin. North Am. 51:701, 1967.
6. Selling, B., and Meilman, E. Acute disseminated encephalomyelitis treated with ACTH. N. Engl. J. Med. 253:275, 1955.
Демиелинизирующее заболевание ЦНС
Демиелинизирующие заболевания головного и спинного мозга – это патологические процессы, приводящие к разрушению миелиновой оболочки нейронов, нарушению передачи импульсов между нервными клетками мозга. Считается, что в основе этиологии заболеваний лежит взаимодействие наследственной предрасположенности организма и определенных факторов внешней среды. Нарушение передачи импульсов приводит к патологическому состоянию центральной нервной системы.
Какие это заболевания
Существуют следующие виды демиелинизирующих заболеваний:
Генетические заболевания
Когда происходит повреждение нервной ткани, организм отвечает реакцией – разрушением миелина. Заболевания, которые сопровождаются разрушением миелина, подразделяются на две группы – миелинокластии и миелинопатии. Миелинокластии – это разрушение оболочки под воздействием внешних факторов. Миелинопатия – это генетически обусловленное разрушение миелина, связанное с биохимическим дефектом строения оболочки нейронов. В то же время, такое распределение на группы считается условным – первые проявления миелинокластии могут говорить о предрасположенности человека к заболеванию, а первые проявления миелинопатии могут быть связаны с повреждениями под воздействием внешних факторов. Рассеянный склероз считают заболеванием людей с генетической предрасположенностью к разрушению оболочки нейронов, с нарушением метаболизма, недостаточностью иммунной системы и наличием медленной инфекции. К генетическим демиелинизирующим заболеваниям относятся: невральная амиотрофия Шарко-Мари-Тута, гипертрофическая невропатия Дежерина-Сотта, диффузный периаксиальный лейкоэнцефалит, болезнь Канавана и многие другие заболевания. Генетические демиелинизирующие заболевания встречаются реже, чем демиелинизирующие заболевания с аутоиммунным характером.
Код по МКБ 10
Демиелинизирующие заболевания головного мозга МКБ 10 имеют коды:
Болезни нервной системы проходят в МКБ 10 под кодом G00-G99. Специалисты считают классификацию по МКБ 10 недостаточно совершенной. Была создана еще одна шкала инвалидизации, которую используют при рассеянном склерозе – EDSS. Такая шкала оценивает все состояния при рассеянном склерозе – походку, равновесие, параличи, самообслуживание и другие факторы. Чтобы пользоваться шкалой врач для оценки состояния пациента сдает специальный экзамен.
Классификация заболеваний
Подострые формы заболевания проявляются в виде заболеваний:
Лечение демиелинизирующих заболеваний нервной системы
Лечение демиелинизирующего заболевания зависит от типа заболевания и степени его тяжести, относится к длительным и сложным процессам. Помимо медикаментозного лечения, больному назначают диету, рекомендуют соблюдать строгий распорядок дня, режим сна и бодрствования, регулярно проходить курс массажа, заниматься лечебной физкультурой. Каждый пациент с демиелинизирующим заболеванием требует индивидуального подхода, поддерживающая терапия пациентов с демиелинизирующим заболеванием занимает долгие годы.
Чем поможет врач Юсуповской больницы
В отделении неврологии Юсуповской больнице работают высококвалифицированные врачи, которые специализируются на лечении демиелинизирующих заболеваний. Врачи постоянно обмениваются знаниями со специалистами других клиник как внутри страны, так и за рубежом. Они посещают конференции на которых знакомятся с современными методиками лечения рассеянного склероза и других заболеваний демиелинизирующей группы.
Специалисты Юсуповской больницы проведут диагностику демиелинизирующего заболевания спинного мозга, головного мозга, назначат эффективное медикаментозное лечение. В больнице можно пройти курс массажа, заниматься лечебной гимнастикой со специалистом. С пациентом и его родственниками работают психологи больницы. В Юсуповской больнице пациент может наблюдаться в течение многих лет, своевременно получать необходимую медицинскую помощь. Записаться на консультацию можно по телефону.
Энцефалопатия
Энцефалопатия – это собирательное название, включающее однотипные поражения головного мозга, возникающие под действием различных причин. Патологический процесс сопровождается гибелью отдельных нейронов и разрушением связей между ними. При отсутствии медицинской помощи приводит к прогрессирующему ухудшению состояния вплоть до полной деградации личности.
Общие сведения
Энцефалопатия возникает на фоне нарушения метаболизма в клетках головного мозга. Вне зависимости от причины, патология протекает по единому сценарию. Сначала происходит снижение активности нейронов, затем – постепенная их гибель. Очаги дистрофии располагаются по всему головному мозгу, что вызывает разнообразную симптоматику.
Повреждения носят необратимый характер, но при своевременном обращении к специалисту и качественном лечении состояние пациента может улучшиться. Оставшиеся неповрежденными нейроны частично берут на себя функцию погибших клеток, и работа головного мозга значительно улучшается. Если заболевание было застигнуто на ранней стадии, пациент сохраняет полную ясность ума.
Причины
Поражение нервных клеток может возникнуть на фоне воздействия разнообразных патологических факторов.
Врачи выделяют врожденную и приобретенную энцефалопатию. Первая возникает на фоне неправильного течения беременности или родов и, зачастую, развивается еще во время пребывания плода в утробе матери. Ее признаки обнаруживаются сразу после родов или появляются в первые недели жизни. Диагностикой и лечением этого состояния занимаются неонатологи и педиатры.
Приобретенная энцефалопатия встречается уже во взрослом возрасте. Она подразделяется на несколько видов в зависимости от причины гибели нейронов:
В зависимости от скорости развития процесса выделяют энцефалопатию острую и хроническую. Первая может развиться в течение нескольких дней или часов, чаще возникает на фоне сильной интоксикации, травмы, инфекционного процесса. Хронический процесс может протекать годами и десятилетиями.
Степени
Границы между степенями тяжести энцефалопатии условны, но для удобства врачи пользуются следующей классификацией:
Симптомы
Признаки энцефалоптии зависят от локализации очага разрушения, а также степени развития заболевания. Наиболее часто пациенты и их родственники сталкиваются со следующими симптомами:
У одних пациентов преобладают расстройства поведения, другие перестают нормально владеть своим телом; у третьих страдают, в основном, органы чувств. В тяжелых случаях человек требует постоянного ухода и наблюдения окружающих.
Осложнения
Осложнения энцефалопатии связаны с сильным и необратимым поражением головного мозга и представляют собой предельную степень наблюдаемых симптомов:
Диагностика
Диагностикой и лечением энцефалопатии занимается врач невролог. Обследование пациента включает в себя:
При необходимости могут быть назначены другие анализы и обследования, а также консультации специалистов для точного определения причины энцефалопатии.
Лечение
Чем раньше будет начато лечение энцефалопатии, тем больше шансов остановить прогрессирование патологии и восстановить полноценную работу головного мозга.
В первую очередь, необходимо устранить причину поражения нейронов:
Лечение непосредственно энцефалопатии требует назначения препаратов, улучшающих кровоток в сосудах головного мозга и обмен веществ внутри клетки. В зависимости от причины и степени поражения, врачи могут назначить:
При энцефалопатии курсы лечения проводятся регулярно, минимум 2 раза в год. Это позволяет держать заболевание под контролем. Подбор конкретных препаратов и определение дозировки осуществляется только врачом. Единой схемы лечения для всех больных не существует.
Для усиления действия лекарственных препаратов используются немедикаментозные методы лечения:
В отдельных случаях (при сосудистой природе энцефалопатии) приходится прибегать к хирургическому лечению:
Профилактика
Энцефалопатия – сложное заболевание. Не существует четкой методики, позволяющей предупредить ее появление и устранить все факторы риска. Врачи рекомендуют придерживаться следующих правил:
Лечение в клинике «Энергия здоровья»
Врачи клиники «Энергия здоровья» всегда готовы принять пациента любого возраста. Мы проведем тщательное обследование, выявим возможные причины энцефалопатии и примем все меры по ее устранению:
Наши неврологи будут контролировать состояние пациента и корректировать лечение при необходимости. Лечение энцефалопатии – это длительный и сложный процесс, но мы готовы за него взяться.
Преимущества клиники
Если Вам требуется полноценное обследование и качественное лечение, добро пожаловать в клинику «Энергия здоровья». Здесь Вас ждут:
Если у Вас или Ваших родственников появились признаки энцефалопатии, не затягивайте с обращением к врачу. Чем будет начато лечение, тем лучше результат. Запишитесь в клинику «Энергия здоровья» и позвольте нашим врачам подобрать оптимальную терапию.
Что такое перинатальная энцефалопатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Гавриловой Татьяны Алексеевны, детского невролога со стажем в 20 лет.
Определение болезни. Причины заболевания
Перинатальная энцефалопатия (перинатальное поражение центральной нервной системы) — это заболевание, которое характеризуется повреждением нервной системы ребёнка в перинатальный период.
Перинатальная энцефалопатия (ПЭП) и перинатальное поражение ЦНС — это равнозначные термины, однако детские неврологи чаще применяют второй вариант при постановке диагноза.
В РФ принято объединять всевозможные варианты поражения нервной системы под одним общим диагнозом – «перинатальная энцефалопатия», а в международной классификации, наоборот, максимально уточнять его название и код.
То есть российскому обобщённому диагнозу «перинатальная энцефалопатия» в МКБ-10 может соответствовать несколько уточнённых диагнозов, например:
Основные факторы, приводящие к повреждению нервной системы во время беременности:
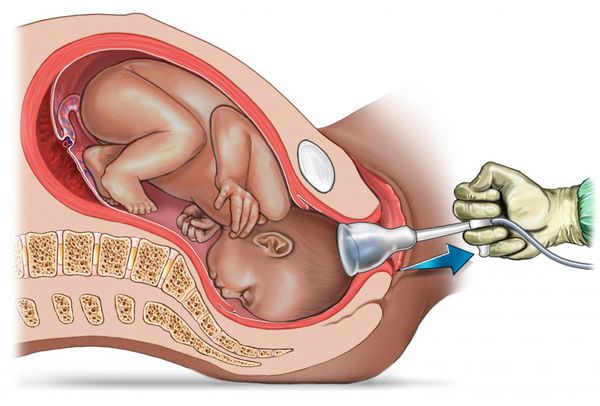
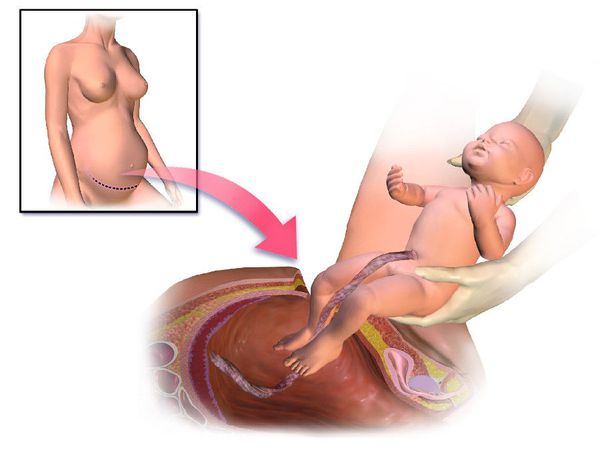
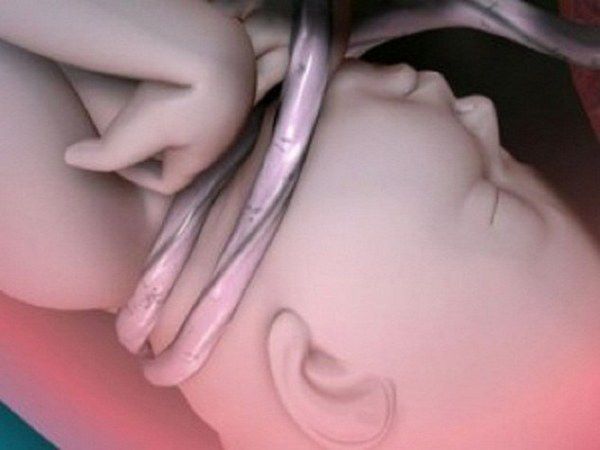
Основные факторы, приводящие к повреждению нервной системы в родах:
Основные факторы, приводящие к повреждению головного мозга после родов:
Симптомы перинатальной энцефалопатии
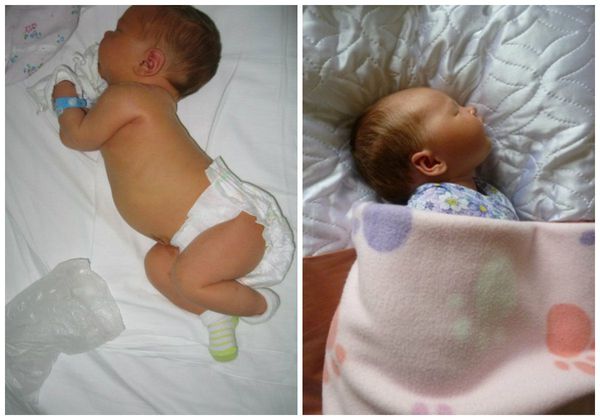
Уже при рождении при наличии тяжёлой родовой травмы с внутричерепным или внутрижелудочковым кровоизлиянием, асфиксией в родах и т. д. у детей отмечаются такие проявления, как угнетение или возбуждение ЦНС, внутричерепная гипертензия (повышенное давление), судороги и даже кома. В таком случае дети экстренно госпитализируются в отделение неонатологии, где получают интенсивное лечение под постоянным наблюдением врачей с внутривенным введением лекарственных препаратов. При необходимости детей временно подключают к аппарату ИВЛ (искусственной вентиляции лёгких).
У детей до года с перинатальной энцефалопатией клинические проявления делят на несколько групп.
Синдром двигательных нарушений:
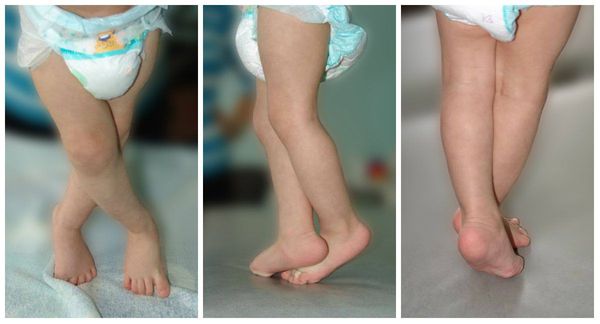
Мышечный тонус при этом может быть повышен либо снижен. При повышении тонуса мышц в руках преобладает тонус в сгибателях (ребёнок держит ручки в кулачках), в ногах преобладает тонус в икроножных мышцах и приводящей группе мышц бедра (при попытке поставить на поверхность ребёнок поджимает пальцы стоп, опора на носочки с перекрёстом).
Также у многих детей с перинатальным поражением ЦНС отмечается задержка психомоторного развития. В связи с чем детский невролог должен чётко знать календарь психомоторного развития у детей до года. При нормальном психомоторном развитии дети начинают:
Существуют индивидуальные особенности развития, небольшие отклонения в развитии могут проходить самостоятельно, но отставание в психомоторном развитии доношенного ребёнка на 2 месяца и более требует осмотра детского невролога для решения вопроса: нуждается ли ребёнок в лечении и назначении комплексной реабилитации.
Не стоит заниматься самолечением, обследование и лечение ребёнку должен назначить детский невролог.
Патогенез перинатальной энцефалопатии
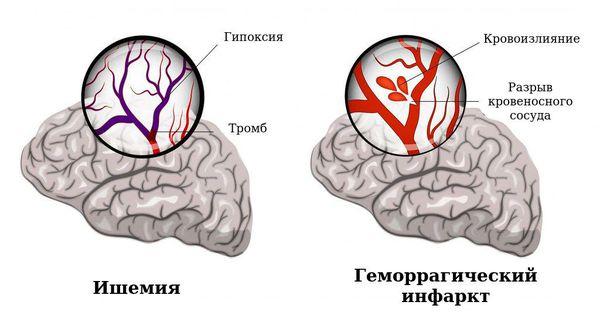
При неблагополучном течении беременности и родов универсальным патогенетическим фактором, повреждающим головной мозг, является гипоксия — это недостаточное поступление кислорода к клеткам головного мозга.
Существует два основных варианта повреждения головного мозга:
Поражение нервной системы при внутриутробных инфекциях сопровождается вовлечением в воспалительный процесс тканей головного мозга и его оболочек (энцефалит, менингит), повышением внутричерепного давления и присоединением судорог.
Возможен также механический перелом ключицы, с повреждением нервного сплетения, расположенного вблизи, возможно механическое повреждение лицевого нерва с формированием в дальнейшем пареза (ослабления) лицевого нерва. При тяжёлых родах возможно формирование ротационного подвывиха шейных позвонков.
Классификация и стадии развития перинатальной энцефалопатии
Перинатальные поражения ЦНС в зависимости от основного повреждающего фактора:
Длительность острого периода:
Восстановительный период длится от месяца до года, у недоношенных детей этот период удлиняется до 2 лет.
Осложнения перинатальной энцефалопатии
В случае тяжёлого поражения нервной системы и несвоевременного начала комплексного лечения впоследствии возможно формирование серьёзных нарушений:
Диагностика перинатальной энцефалопатии
В тех случаях, когда неврологические нарушения были ярко выражены изначально, диагноз перинатальной энцефалопатии устанавливается непосредственно в роддоме и ребёнок своевременно направляется в отделение неонатологии для интенсивной терапии.
В таком случае диагноз ставится на основании:
Далее невролог назначает ребёнку обследование:
При осмотре глазного дна отмечается ангиопатия сосудов глазного дна: сужение артерий, расширение и патологическая извитость вен. Однако провести осмотр глазного дна у маленького ребёнка не всегда удаётся, так как он не может зафиксировать взор в нужную для осмотра точку.
Лечение перинатальной энцефалопатии
Лечение перинатальной патологии в острый период проводится в отделении неонатологии.
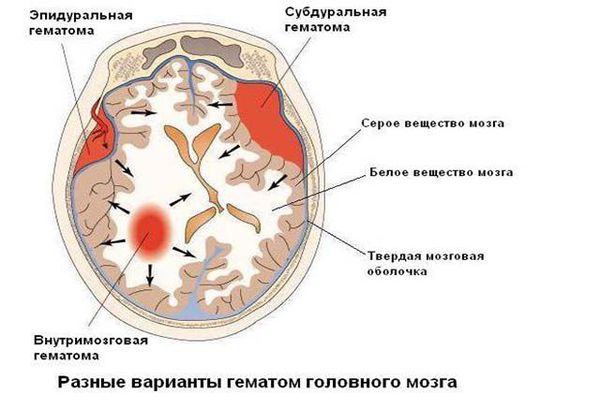
Оперативное лечение может понадобиться при наличии у ребёнка большой гематомы внутри полости черепа — её удаление возможно только хирургическим путём.
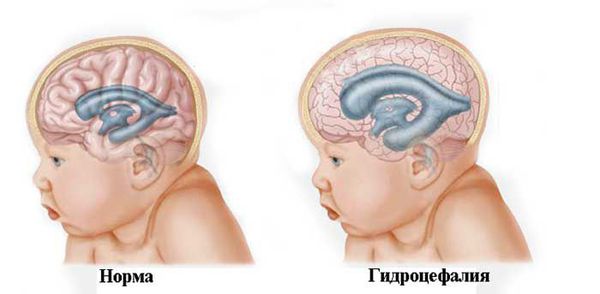
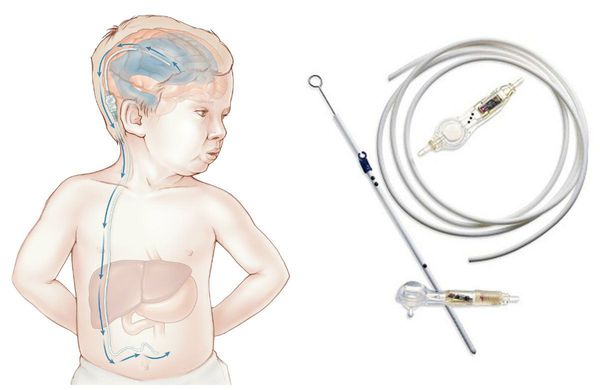
При нарастающей закрытой гидроцефалии, чтобы избежать атрофии головного мозга от сдавления его жидкостью, детям проводят шунтирующую операцию — устанавливают шунт (пластиковую трубочку, по которой лишняя жидкость из полости черепа отводится в брюшную полость и там всасывается).
Однако большинство родителей сталкивается с необходимостью лечения ребёнка с перинатальной энцефалопатией в восстановительный период до 1 года в связи с нарушением мышечного тонуса, задержкой развития, гипертензионно-гидроцефальным синдромом и прочими проявлениями.
Наибольшего эффекта можно добиться с помощью комплексного лечебного подхода.
ЛФК — лечебная физкультура. Может включать различные виды:
Микротоковая рефлексотерапия (МТРТ) — новая медицинская технология, разрешённая Минздравом РФ и рекомендованная для лечения детей с органическим поражением головного мозга, с задержками развития двигательного, речевого, психического развития и ДЦП. Лечение проводится в амбулаторном режиме в реабилитационных центрах в различных регионах РФ.
Лечебное воздействие физиологичное и безболезненное, оказывается токами микроамперного диапазона на нейрорефлекторные зоны на различных участках кожного покрова. Микротоки в 10 раз меньшие, чем при стандартной физиотерапии. Лечение проводится по индивидуальной схеме с учётом всех имеющихся у ребёнка проявлений перинатальной энцефалопатии.
В процессе лечения восстанавливается нормальная рефлекторная деятельность головного мозга, нормализуется мышечный тонус: спастичные (напряжённые) мышцы — расслабляются, гипотоничные (ослабленные) — стимулируются. МТРТ стабилизирует тонус сосудов головного мозга, что позволяет скомпенсировать внутричерепное давление.
Мочегонные препараты целесообразно использовать только при повышении внутричерепного давления (расширение ликворных пространств на НСГ, наличие клинических проявлений гипертензионно-гидроцефального синдрома).
Прогноз. Профилактика
В качестве профилактики необходимо минимизировать факторы риска при беременности и родоразрешении. Важнейшей задачей является предупреждение внутриутробной гипоксии. Для этого важно провести адекватную терапию имеющихся хронических заболеваний и своевременную коррекцию течения осложнённой беременности.
К вопросу диагностики и лечения психовегетативных расстройств в общесоматической практике
Более чем у 25% пациентов общесоматической сети имеет место психовегетативный синдром как наиболее частый вариант синдрома вегетативной дистонии (СВД), за которым стоят тревога, депрессия, а также нарушения адаптации, которые врачи устанавливают на синдро
Более чем у 25% пациентов общесоматической сети имеет место психовегетативный синдром как наиболее частый вариант синдрома вегетативной дистонии (СВД), за которым стоят тревога, депрессия, а также нарушения адаптации, которые врачи устанавливают на синдромальном уровне. Однако часто проявления психовегетативного синдрома ошибочно диагностируются как соматическая патология. Этому в свою очередь способствуют приверженность соматическому диагнозу как самих врачей, так и пациентов, а также особая клиническая картина соматизации психических расстройств в клинике внутренних болезней, когда за множеством соматических и вегетативных жалоб трудно выявить психопатологию, которая зачастую бывает субклинически выраженной. В последующем неправильная диагностика с установкой соматического диагноза и игнорированием психических расстройств приводит к неадекватному лечению, что проявляется не только в назначении неэффективных групп препаратов (бета-блокаторы, блокаторы кальциевых каналов, ноотропы, метаболики, сосудистые препараты, витамины), но также в проведении слишком коротких курсов терапии психотропными средствами. В статье приводятся конкретные рекомендации по преодолению подобных трудностей.
Психическая патология широко распространена среди пациентов первичной медицинской сети и часто представлена в виде депрессивных и тревожных расстройств, включая стрессовые реакции и расстройства адаптации, соматоформные расстройства [1]. По данным российской эпидемиологической программы КОМПАС распространенность депрессивных расстройств в общемедицинской практике колеблется от 24% до 64%. При этом у пациентов, однократно обратившихся в поликлинику в течение года, расстройства аффективного спектра выявляются в 33% случаев, обратившихся более пяти раз — в 62%, а также среди женщин чаще, чем среди мужчин [2].
Получены аналогичные данные о высокой распространенности тревожных и соматоформных расстройств в первичной сети [3–5]. Стоит отметить, что врачам общей практики за множеством соматических и вегетативных жалоб пациентов трудно выявить психопатологию, которая зачастую бывает субклинически выраженной и не полностью удовлетворяет диагностическим критериям психического расстройства [6], однако приводит к значимому снижению качества жизни, профессиональной и социальной активности [7–9] и имеет широкое распространение в популяции. По данным российских и зарубежных исследователей около 50% индивидуумов в обществе имеют либо пороговые, либо субпороговые расстройства [2, 10–12]. В зарубежной литературе для обозначения подобных пациентов был предложен термин «Medical Unexplained Symptoms», что буквально означает «С медицинской точки зрения необъяснимые симптомы» (МНС).
В настоящее время этот термин заменяет понятие «соматизация» и является наиболее приемлемым для описания большой группы пациентов, физические жалобы которых не верифицируются традиционными диагнозами [13]. МНС широко распространены во всех медицинских учреждениях. До 29% пациентов общесоматических клиник имеют субпороговые проявления тревоги и депрессии в виде соматических симптомов, которые сложно объяснить имеющимися соматическими заболеваниями [14], и их выделение оспаривается многочисленными перекрестными и синдромальными диагнозами [15]. В России и странах СНГ врачи в своей практике активно используют термин «СВД», под которым большинство практикующих врачей понимают психогенно обусловленные полисистемные вегетативные нарушения [16]. Именно психовегетативный синдром определяется как наиболее частый вариант СВД, за которым стоят тревога, депрессия, а также нарушения адаптации, которые врачи устанавливают на синдромальном уровне.
В подобных случаях речь идет о соматизированных формах психопатологии, когда пациенты считают себя соматически больными и обращаются к врачам терапевтических специальностей [17]. Несмотря на то, что как таковой нозологической единицы СВД не существует, на отдельных территориях России объем диагноза «СВД» составляет 20–30% от всего объема зарегистрированных данных о заболеваемости, и при отсутствии необходимости направлять больного на консультацию в специализированные психиатрические учреждения он кодируется врачами и статистиками амбулаторно-поликлинических учреждений как соматический диагноз [18]. По результатам опроса 206 врачей-неврологов и терапевтов России, участников конференций, проводимых Отделом патологии вегетативной нервной системы НИЦ и Кафедрой нервных болезней ФППОВ Первого Московского государственного медицинского университета им И. М. Сеченова за период 2009–2010 гг., 97% опрошенных применяют диагноз «СВД» в своей практике, из них 64% используют его постоянно и часто.
По нашим данным более чем в 70% случаев СВД выносится в основной диагноз под грифом соматической нозологии G90.9 — расстройство вегетативной (автономной) нервной системы неутонченное или G90.8 — другие расстройства вегетативной нервной системы. Однако в реальной практике имеет место недооценка сопутствующих соматических расстройств психопатологии. Применение «Опросника для выявления вегетативной дисфункции» [16] у 1053 амбулаторных пациентов с признаками вегетативной дисфункции позволило установить, что у большей части пациентов (53% больных) имеющийся вегетативный дисбаланс рассматривался в рамках таких соматических заболеваний, как «дисциркуляторная энцефалопатия», «дорсопатия» или «черепно-мозговая травма и ее последствия».
Менее чем у половины обследованных (47% больных) наряду с соматовегетативными симптомами были выявлены сопутствующие эмоционально-аффективные расстройства преимущественно в виде патологической тревоги, которая у 40% указанных больных была диагностирована как вегетососудистая дистония, у 27% — как невроз или невротические реакции, у 15% — как неврастения, у 12% — как панические атаки, у 5% — как соматоформная дисфункция вегетативной нервной системы и у 2% — как тревожное расстройство.
Наши результаты соотносятся с данными, полученными в спланированных эпидемиологических исследованиях по оценке распространенности и диагностике тревоги и депрессии врачами общей практики, что еще раз подчеркивает широкую представленность соматизированных форм психопатологии [17], а также их частое игнорирование врачами общей практики [2, 19]. Подобная гиподиагностика связана, во-первых, со сложившейся системой организации помощи, когда отсутствуют четкие диагностические критерии для обозначения проявлений несоматического происхождения, что приводит к последующим трудностям в объяснении симптомов, а также невозможность применения диагнозов психиатрического круга врачами общей практики.
Во-вторых, наряду с нежеланием пациентов иметь психиатрический диагноз и отказа их лечиться у психиатров имеет место недооценка практикующими врачами роли психотравмирующих ситуаций [19]. В итоге гиподиагностика психопатологии, приверженность соматическому диагнозу и игнорирование сопутствующих психических расстройств лежат в основе неадекватной терапии пациентов с психовегетативным синдромом. Значительный вклад в гиподиагностику вносят особенности клинической картины, а именно соматизация психических расстройств в клинике внутренних болезней, когда за множеством соматических и вегетативных жалоб трудно выявить психопатологию, которая зачастую бывает субклинически выраженной и не полностью удовлетворяет диагностическим критериям психического расстройства [6]. В большинстве случаев врачи не рассматривают эти состояния как патологические и не лечат их [20, 21], что способствует хронизации психопатологии вплоть до достижения развернутых психопатологических синдромов [22].
Учитывая, что врачи общей практики выделяют соматовегетативные проявления тревоги и депрессии на синдромальном уровне в виде СВД, а также невозможность на практике применения психиатрических диагнозов, на первом этапе ведения большого числа пациентов становится возможной синдромальная диагностика психовегетативного синдрома, которая включает в себя:
Учитывая, что вегетативная дисфункция является обязательным синдромом и включена в диагностические критерии большинства тревожных расстройств: патологической тревоги (паническое, генерализованное, смешанное тревожно-депрессивное расстройство), фобий (агорафобия, специфические и социальные фобии), реакций на стрессовый раздражитель, врачу важно оценить психические расстройства: уровень тревоги, депрессии с помощью психометрического тестирования (например, использование валидизированной в России психометрической шкалы: «Госпитальная шкала тревоги и депрессии» (см. табл. на стр. 49) [23]).
Назначение адекватной терапии требует от врача необходимости в информировании пациента о сути болезни, ее причинах, возможности терапии и прогноза. Представления пациента о собственном заболевании определяют его поведение и обращение за помощью. Так, например, если имеющиеся проявления психовегетативного синдрома пациент рассматривает не как соматическое заболевание, а в рамках социальных проблем и особенностей черт характера, предпочтение в лечении будет отдаваться собственным усилиям, непрофессиональным методам и самолечению. В ситуации, когда пациент рассматривает существующие у него симптомы как результат соматического страдания и поражения нервной системы, имеет место обращение за медицинской помощью к врачу-неврологу или терапевту. Существуют так называемые «уязвимые» группы людей с высоким риском формирования психовегетативного синдрома. Среди множества факторов выделяют следующие основные:
Наличие вышеперечисленных факторов в сочетании с клиническими проявлениями позволяет врачу разъяснить пациенту суть заболевания и аргументировать необходимость назначения психотропной терапии.
На этапе выбора оптимальной тактики лечения и принятии решения о моно- или политерапии необходимо придерживаться рекомендаций в лечении пациентов с психовегетативными расстройствами. Существующие в настоящее время стандарты терапии пациентов с СВД и, в частности, с диагнозом, определяемым кодом МКБ-10 G90.8 или G90.9, наряду с ганглиоблокаторами, ангиопротекторами, вазоактивными средствами рекомендуют применение седативных препаратов, транквилизаторов, антидепрессантов, малых нейролептиков [24]. Следует отметить, что большинство симптоматических препаратов оказываются неэффективными в терапии психовегетативного синдрома. К таковым относятся бета-блокаторы, блокаторы кальциевых каналов, ноотропы, метаболики, сосудистые препараты, витамины. Однако по данным проведенного среди врачей опроса нами было установлено, что до сих пор большая часть врачей предпочитают использовать сосудисто-метаболическую терапию (83% терапевтов и 81% неврологов), бета-адреноблокаторы (около половины врачей). Из противотревожных средств у 90% терапевтов и 78% неврологов до сих пор остаются популярными седативные травяные сборы. Антидепрессанты используют 62% терапевтов и 78% неврологов. Малые нейролептики применяют 26% терапевтов и 41% неврологов.
Учитывая, что психовегетативный синдром — частое проявление хронической тревоги, в основе которой лежит нарушение баланса ряда нейромедиаторов (серотонина, норадреналина, ГАМК и других), пациенты нуждаются в назначении психотропных препаратов. Оптимальными средствами в данной ситуации являются ГАМКергические, серотонин-, норадреналинергические или препараты со множественным действием.
Из ГАМКергических препаратов наиболее подходящими можно назвать бензодиазепины. Однако по профилю переносимости и безопасности данная группа не является средствами первой линии выбора. Высокопотенциальные бензодиазепины, такие как алпразолам, клоназепам, лоразепам, широко применяются в терапии пациентов с патологической тревогой. Им свойственны быстрое начало действия, они не вызывают обострения тревоги на начальных этапах терапии (в отличие от селективных ингибиторов обратного захвата серотонина), но при этом не лишены недостатков, свойственных всем бензодиазепинам: развитие седации, потенцирование действия алкоголя (который часто принимается больными с тревожно-депрессивными расстройствами), формирование зависимости и синдром отмены, а также недостаточное влияние на коморбидные тревоге симптомы. Это обуславливает возможность применения бензодиазепинов только короткими курсами. В настоящее время препараты рекомендуются в качестве «бензодиазепинового моста» — в первые 2–3 недели инициального периода терапии антидепрессантами.
Препараты, влияющие на активность моноаминергической передачи, являются приоритетными в выборе фармакотерапии. К современным средствам первого выбора для лечения патологической тревоги относятся антидепрессанты из группы селективных ингибиторов обратного захвата серотонина (СИОЗС), т. к. преимущественно дефицит данного нейромедиатора реализует психовегетативные проявления патологической тревоги [5]. СИОЗС характеризуются широким спектром терапевтических возможностей при достаточно высокой безопасности при длительной терапии. Однако, несмотря на все свои положительные стороны, СИОЗ имеют и ряд недостатков. Среди побочных эффектов отмечаются обострение тревоги, тошнота, головные боли, головокружение в течение первых нескольких недель лечения, а также недостаточная их эффективность у части пациентов. У пожилых людей СИОЗС могут приводить к нежелательным взаимодействиям. СИОЗС не следует назначать пациентам, принимающим НПВП, т. к. увеличивается риск гастроинтестинального кровотечения, а также пациентам, принимающим варфарин, гепарин, т. к. усиливается антитромботический эффект с угрозой кровотечения.
Антидепрессанты двойного действия и трициклические антидепрессанты являются наиболее эффективными препаратами. В неврологической практике данные препараты и, в частности, селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН) показали высокую эффективность у пациентов, страдающих хроническими болевыми синдромами различной локализации [25–29]. Однако наряду с большим спектром положительных влияний с повышением эффективности может ухудшаться профиль переносимости и безопасности, что и определяет широкий перечень противопоказаний и побочных эффектов СИОЗСН, а также необходимость титрования дозы, что ограничивает их применение в общесоматической сети.
Среди препаратов со множественным действием внимания заслуживают малые нейролептики, особенно Тералиджен® (алимемазин), характеризующийся благоприятным профилем эффективности и безопасности. Широкий спектр его действия обусловлен модулирующим влиянием на центральные и периферические рецепторы. Блокада дофаминовых рецепторов триггерной зоны рвотного и кашлевого центра ствола головного мозга реализуется в противорвотном и противокашлевом действии, что обуславливает применение Тералиджена® в лечении рвоты у детей в послеоперационном периоде [30]. Его слабое влияние на блокаду D2-рецепторов мезолимбической и мезокортикальной системы приводит к тому, что он оказывает мягкое антипсихотическое действие. Однако при этом он не вызывает тяжелых побочных эффектов в виде ятрогенной гиперпролактинемии и экстарапирамидной недостаточности, наблюдаемых при назначении других малых и больших нейролептиков [31].
Блокада Н1-гистаминовых рецепторов в ЦНС приводит к развитию седативного эффекта и использованию препарата в лечении нарушений сна у взрослых и детей [32], на периферии — в противозудном и противоаллергическом влиянии, что нашло свое применение в лечении «зудящих» дерматозов» [33]. Блокада альфа-адренорецепторов ретикулярной формации ствола головного мозга оказывает седативный эффект, а голубого пятна и его связей с миндалевидным телом — способствует редукции тревоги и страха [34]. Сочетание блокады периферических альфа-адренорецепторов (что реализуется в гипотензивном эффекте) и М-холинорецепторов (что проявляется в спазмолитическом действии) широко применяется с целью премедикации в хирургии и стоматологии [35], в лечении болевого синдрома. Трициклическое строение алимемазина также определяет его антидепрессивное действие за счет воздействия на пресинаптические рецепторы и усиления дофаминергической передачи [36].
Результаты собственных исследований по оценке эффективности Тералиджена® (в дозе 15 мг/сутки, разделенной на три приема, в течение 8 недель терапии), полученные у 1053 амбулаторных неврологических пациентов с вегетативной дисфункцией, продемонстрировали его значимый терапевтический эффект в виде положительной динамики по «Вопроснику для выявления вегетативных изменений» (см. табл. на стр. 48) и редукции соматовегетативных жалоб. Большую часть пациентов перестали беспокоить ощущения сердцебиения, «замирания» или «остановки сердца», чувство нехватки воздуха и учащенное дыхание, желудочно-кишечный дискомфорт, «вздутия» и боли в животе, а также головные боли по типу напряже. На этом фоне имело место повышение работоспособности. Пациенты стали быстрее засыпать, сон стал более глубоким и без частых ночных пробуждений, что в целом свидетельствовало об улучшении качества ночного сна и способствовало ощущению выспанности и бодрости при пробуждении утром (табл. 1).
Имеющийся у алимемазина благоприятный профиль эффективности и переносимости позволяет широко применять Тералиджен® у пациентов с психовегетативным синдромом в средней терапевтической дозе 15 мг/сутки, разделенной на три приема. Важным фактором хорошей комплаентности является назначение Тералиджена® по следующей схеме: первые четыре дня назначают по 1/2 таблетке на ночь, в течение последующих четырех дней — по 1 таблетке на ночь, далее каждые четыре дня прибавляется по 1 таблетке в утреннее время и через четыре дня в дневное время. Таким образом, через 10 дней пациент принимает полноценную терапевтическую дозу препарата (табл. 2).
Также алимемазин (Тералиджен®) показан в качестве дополнительной терапии при:
Терапия психотропными препаратами требует назначения адекватной дозы, оценки переносимости и полноты соблюдения пациентами режима терапии. Необходимо назначать полную терапевтическую дозу психотропных препаратов для купирования тревожных, депрессивных и смешанных тревожно-депрессивных нарушений. Учитывая сложности ведения пациентов в инициальном периоде лечения, рекомендуется использование «бензодиазепинового моста» в первые 2–3 недели терапии антидепрессантами из класса СИОЗС или СИОЗСН. Также рекомендуются комбинирование СИОЗС с малыми нейролептиками (в частности, с алимемазином), которые влияют на широкий спектр эмоциональных и соматических симптомов (в особенности на болевые ощущения). Подобные комбинации заключают в себе потенциал для более быстрого начала антидепрессивного эффекта, а также повышают вероятность ремиссии.
Врачи общей практики часто сталкиваются с трудностями по определению продолжительности курсового лечения. Это связано с недостатком информации об оптимальном сроке лечения и отсутствием стандартов длительности лечения пациентов с психовегетативным синдромом. Важно, что короткие курсы длительностью 1–3 месяца чаще приводят к последующему обострению, чем длительные (6 месяцев и более). Учитывая подобные сложности, для практикующего врача можно рекомендовать следующую схему терапии:
Выбор тактики отмены базисного препарата зависит, в первую очередь, от психологического настроя пациента. Отмена препарата может происходить резко, так называемый «обрыв» лечения. Однако при наличии у больного страха перед отменой длительно принимаемого средства сама отмена препарата может вызвать ухудшение состояния. В подобных ситуациях рекомендуют постепенную отмену (градуиированная отмена) или перевод пациента на «мягкие» анксиолитики, в том числе растительные средства.
Литература
Е. С. Акарачкова, кандидат медицинских наук
Первый МГМУ им. И. М. Сеченова, Москва