С чем реагирует оксид серебра
С чем реагирует оксид серебра
Имеет выраженные основные свойства. В воде плохо растворяется, но придает ей слабощелочную реакцию:
При нагревании до 300°С разлагается на кислород и серебро:
С щелочами не взаимодействует, в водных растворах аммиака образует гидроксид диамминсеребра (I):
В разбавленной серной кислоте растворяется, образуя сульфат серебра (I):
Проявляет окислительные свойства, особенно по отношению к некоторым органическим веществам:
HCHO + 2Ag2O 
Оксид серебра (I) получают осторожным нагреванием гидроксида серебра:
Гидроксид серебра (I) AgOH не выделен в индивидуальном виде, это неустойчивое соединение, из растворов не образуется. При взаимодействии солей серебра (I) с щелочами в растворе образуется гидратированный оксид Ag2O·nH2O.
6.8. Обнаружение ионов серебра (I)
Ионы серебра (I) в растворе можно обнаружить при приливании раствора, содержащего хлорид-ионы 
наблюдается выпадение характерного белого творожистого осадка.
Оксид серебра I
| Оксид серебра I | |
|---|---|
| Систематическое наименование | оксид серебра I |
| Хим. формула | Ag2O |
| Молярная масса | 231.735 г/моль |
| Плотность | 7,14 г/см³ |
| Температура | |
| • плавления | 280 |
| Мол. теплоёмк. | 65.9 Дж/(моль·К) |
| Растворимость | |
| • в воде | 0.0025 |
| Рег. номер CAS | 20667-12-3 |
| PubChem | 9794626 |
| Рег. номер EINECS | 243-957-1 |
| SMILES | |
| RTECS | VW4900000 |
| ChemSpider | 7970393 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Оксид серебра I — химическое соединение с формулой Ag2O.
Содержание
Получение
Оксид может быть получен взаимодействием нитрата серебра с щёлочью в водном растворе:
Это связано с тем, что образующийся в ходе реакции гидроксид серебра I быстро разлагается на оксид и воду:
Более чистый оксид серебра I может быть получен в результате анодного окисления металлического серебра в дистиллированной воде.
Свойства
Свежий осадок Ag2O легко взаимодействует с кислотами:
Обладает фоточувствительностью. При температуре выше 280 °C разлагается.
Оксид серебра Ag2O и его свойства

Основные свойства оксида серебра (Ag2O)
Реакция оксида серебра (I) с кислотами
Оксид серебра (I), растворяясь в разбавленной серной кислоте, образует сульфат серебра (I):
Ag2O + H2SO4 (разб.) = Ag2SO4 + H2O
Что произойдет с оксидом серебра (I), если его нагреть до температуры 300 градусов?
При нагревании оксида серебра (I) до 300 градусов он разлагается на элементы серебро и кислород:
Растворимость оксида серебра (I) в воде
Оксид серебра (I), плохо растворяется в воде и придает ей слабощелочную реакцию:
Ag2O + H2O = 2Ag+ + 2OH-
Оксид серебра растворяется в плавиковой и азотной кислотах, в солях аммония, в растворах цианидов щелочных металлов, в аммиаке и т. д.
Ag2O + 2HF = 2AgF + Н2О
Ag2O + 2HNO3 = 2AgNO3 + Н2О
Получение оксида серебра (I)
Получить оксид серебра (I) можно взаимодействием нитрата серебра со щёлочью в водном растворе:
Получить оксид серебра (I) можно так же обработкой раствора AgNO3 растворами гидроксидов щелочноземельных металлов:
2AgNO3 + 2KOH = Ag2O + 2KNO3 + H2O
Чистый оксид серебра (I) может быть получен в результате анодного окисления металлического серебра в дистиллированной воде.
Оксид серебра (I) можно получить, если осторожно нагревать гидроксид серебра:
Водород, оксид углерода, перекись водорода и многие металлы восстанавливают оксид серебра (Ag2О) в водной суспензии до металлического серебра (Ag):
Ag2О + H2 ( при температуре 40 градусов) = 2Ag + Н2О
Ag2О + CO = 2Ag + CO2
Ag2О + H2O2 = 2Ag + H2O + O2
Применение оксида серебра (I)
Оксид серебра может быть источником атомарного кислорода необходимого для зарядки кислородных пистолетов, предназначенных для испытания прочности некоторых материалов на их стойкость к окислению, необходимых для постройки космических аппаратов.
Оксида серебра (I) это очень важное химическое соединение, которое может использоваться в фармацевтической промышленности как антисептик, а так же в производстве стекла и применятся как краситель. Он так же применяется в производстве серебряно-цинковых аккумуляторов, в которых анод представляет собой оксид серебра (I).
Плоские кнопочные батарейки на основе оксида серебра используются, как элементы питания для наручных часов.

Оксид серебра используется в художественных цехах для изготовления новогодних елочных игрушек, например при изготовлении елочных шаров. В цехе стеклодувов внутрь шарика вливают раствор из оксида серебра, аммиака и дистиллированной воды. Потом шарик со смесью взбалтывают, чтобы равномерно окрасились все внутренние стенки игрушки и опускают в воду с температурой 40 градусов. Сначала шарик чернеет, а потом становится серебристым.

Окисление серебра до оксида серебра (I)
Чистое серебро по своей природе это малоактивный металл, который при обычной комнатной температуре, не окисляется на воздухе. Поэтому чистое серебро относится к разряду благородных металлов. Однако это не означает, что серебро вообще не может растворять в себе кислород. Серебро способно при нагревании или расплавлении поглощать значительные объемы кислорода. Даже твердое серебро при температуре 450 градусов способно растворить в себе до пяти объемов кислорода, а при расплавлении металла (при температуре плавления 960 градусов), когда серебро переходит в жидкое состояние, оно способно поглотить двадцатикратный объем кислорода. При остывании жидкого серебра наблюдается явление разбрызгивание металла. Это очень красивая, но опасная реакция, которая была известна человечеству еще в глубокой древности. Опасность разбрызгивания серебра объясняется тем, что когда серебро после расплавления начинает остывать, металл резко начинает высвобождать большое количество кислорода, что и создает эффект брызг металла.
Почему серебро темнеет?
При температуре 170 градусов по Цельсию, серебро на воздухе начинает покрываться тонкой оксидной пленкой, которая представляет собой оксид серебра (Ag2О), а под действием озона образуются высшие оксиды серебра: Ag2О2, Ag2О3. Однако причиной почернения серебра при обычных условиях является не оксид серебра (Ag2О), как некоторые люди ошибочно себе представляют, а образование на поверхности серебра тонкого слоя сульфида серебра (Ag2S). Образование сульфида серебра на поверхности серебряного изделия является следствием взаимодействия благородного металла с серой, которая всегда присутствует в составе сероводорода (H2S). Реакция серебра и сероводорода хорошо протекает в присутствии влаги:
4Ag + 2H2S + O2 = 2Ag2S + 2H2O
При этом серебро может не только потускнеть, но и почернеть. А из-за неровностей, которые может иметь серебро, такая темная пленка при игре света, может показаться даже радужной. Чем толще становится пленка, тем темнее делается серебро. Постепенно пленка темнеет, приобретая коричневый оттенок, а потом она со временем становится черной.
Сульфид серебра (Ag2S) это неорганическое вещество, соль серебра и сероводородной кислоты, твердое вещество серо-чёрного цвета. Эта соль серебра считается одним из химических соединений серебра, которое наименее всего растворимо в воде. Очень тонкий слой сульфида серебра (Ag2S) на поверхности серебряных изделий, придает им розоватую окраску. Сульфид серебра (Ag2S) это очень трудно растворимое химическое соединение. При обычной комнатной температуре эта соль серебра не реагирует даже с кислотами. Только после нагревания сульфид серебра (I) может раствориться в концентрированной азотной кислоте. Сульфид серебра (I) при комнатной температуре может переходить в раствор за счет образования комплексных соединений серебра при растворении его в растворах цианидов.
Чистое серебро редко применяется в изготовлении ювелирных изделий. Чаще всего серебро представлено в виде сплавов. Недостатком этих сплавов серебра заключается в том, что они содержат разные примеси других металлов, например медь. Серебро, соединяясь в присутствии влаги с сероводородом, образует на своей поверхности тонкий темный слой сульфида серебра (Ag2S). А медь, являющаяся вторым компонентом сплава серебра, образует сильфид меди (Cu2S), который имеет так же темный цвет, как и сульфид серебра (I). Кроме того медь может реагировать с кислородом, образуя оксид меди. Поэтому изделия из серебра изготовленные из такого сплава серебра и меди, вследствие коррозии, могут иметь не только темный цвет, но и приобретать красновато-коричневый оттенок. Серебро, со временем, пребывая на воздухе сначала становиться желтоватым, затем делается коричневым, грязно-синим, а потом темнеет. Интенсивность потемнения серебра, зависит от процентного содержания меди в серебряном сплаве. Чем меди больше в серебряно-медном сплаве, тем быстрее идет процесс почернения серебра.
На этом фото изображено столовое серебро (ложки, вилки) которое заметно пожелтело и слегка потемнело. Причиной изменение цвета, является образование на поверхности изделий сульфида серебра и меди, а также оксида меди.
Оксидированное серебро
Для того чтобы серебро не разрушалось, его покрывают тонким слоем оксида серебра. Такое серебро называется оксидированным, то есть покрытым слоем оксида серебра. Такая тонкая оксидная пленка защищает металл от потускнения и улучшает декоративные свойства ювелирных изделий.
На фото выше приведен пример ювелирного серебряного изделия (стильные швензы с оксидированным цветком подсолнуха), выполненного из высокопробного сплава 925 пробы серебра. Данное изделие представляет собой оксидированное серебро 925. Оксид серебра, покрывающий это изделие, надежно защищает серебро от потускнения. Такое оксидированное серебро может долго храниться и не подвергаться дальнейшему окислению. Данное изделие отлично смотрится и имеет великолепный эстетический вид.
На этих фото изображены ювелирные изделия из серебра покрытые тонким слоем оксида серебра: винтажный элемент «Осьминог» (оксид серебра) и оксидированный винтажный элемент «Скарабей».

На этом фото изображены часы-амулет. Это ювелирное изделие выполнено из высокопробного серебра. Часы оксидированы, имеют чеканку с рисунком на корпусе.

На фото слева изображена симпатичная филигрань, винтажный элемент, с замысловатым орнаментом, где центральные лепестки имеют выпуклую форму. Данное ювелирное изделие выполнено из высококачественного сплава, представляет собой серебро 925 пробы и покрыто тонким слоем оксида серебра. На фото справа изображена ладанка «Св. Николай Чудотворец». Материалом, из которого изготовлено данное изделие, является серебро 925 пробы, покрытое тонким слоем оксида серебра.
Структура оксида серебра (Ag2O), свойства, номенклатура и применение
Например, на изображении выше вы можете увидеть ржавую серебряную чашку. Обратите внимание на его почерневшую поверхность, хотя он все еще сохраняет некоторый декоративный блеск; поэтому даже ржавые серебряные предметы можно считать достаточно привлекательными для декоративного использования.
Свойства оксида серебра таковы, что они не портят, на первый взгляд, первоначальную металлическую поверхность. Это сформировано при комнатной температуре простым контактом с кислородом в воздухе; и что еще интереснее, он может разлагаться при высоких температурах (выше 200 ° C).
Это означает, что если удерживать стекло изображения и применять тепло интенсивного пламени, оно восстановит свой серебристый блеск. Следовательно, его образование является термодинамически обратимым процессом..
Оксид серебра также имеет другие свойства и, помимо своей простой формулы Ag2Или это охватывает сложные структурные организации и богатое разнообразие твердых веществ. Тем не менее, Ag2Или это возможно, рядом с Ag2О3, самый представительный из оксидов серебра.
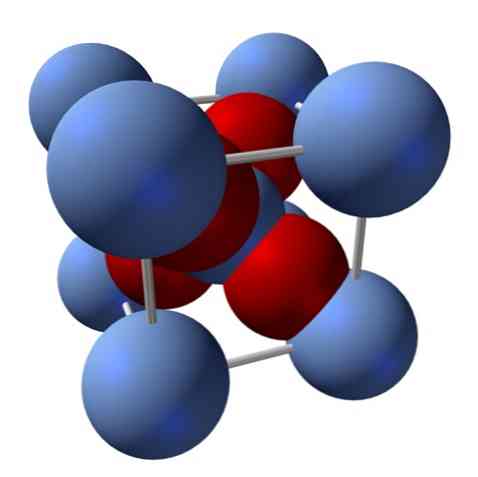
Структура оксида серебра
Например, на верхнем изображении у вас есть элементарная ячейка для кубической кристаллической системы: катионы Ag + серебристо-синие сферы, а O 2- красноватые сферы.
Если вы посчитаете количество сфер, вы обнаружите, что на первый взгляд есть девять серебристо-голубых и четыре красных цвета. Однако принимаются во внимание только фрагменты сфер, содержащихся в кубе; считая их, как доли от общего количества сфер, нужно соблюдать соотношение 2: 1 для Ag2О.
Изменения в количестве Валенсии
Вышесказанное было подтверждено несколькими исследованиями его ионной структуры.
Физико-химические свойства
Если вы поцарапаете поверхность серебряного стакана основного изображения, вы получите твердое тело, которое не только черного цвета, но также имеет коричневые или коричневые тона (верхнее изображение). Некоторые из его физических и химических свойств, о которых сообщают моменты, следующие:
Молекулярный вес
внешний вид
Твердый черный коричневый в виде порошка (обратите внимание, что, несмотря на то, что он является ионным твердым веществом, он не имеет кристаллического вида). Он не имеет запаха и смешан с водой, придает ему металлический привкус
плотность
Точка плавления
277-300 ° С Конечно, он плавится в твердое серебро; то есть он, вероятно, разрушается до образования жидкого оксида.
КПС
растворимость
Если вы внимательно посмотрите на изображение его структуры, вы обнаружите, что сферы Ag 2+ и O 2- Они не расходятся почти по размеру. В результате только небольшие молекулы могут проникать внутрь кристаллической решетки, делая ее нерастворимой почти во всех растворителях; за исключением тех, где он реагирует, таких как основания и кислоты.
Ковалентный персонаж
Хотя неоднократно говорилось, что оксид серебра является ионным соединением, некоторые свойства, такие как его низкая температура плавления, противоречат этому утверждению..
Конечно, рассмотрение ковалентного характера не нарушает того, что объясняется для его структуры, было бы достаточно, чтобы добавить его к структуре Ag2Или модель сфер и стержней для обозначения ковалентных связей.
Также тетраэдры и квадратные плоскости AgO4, как и линии AgOAg, они будут связаны ковалентными (или ковалентными ионными) связями.
Имея это в виду, Ag2Или это на самом деле полимер. Тем не менее, рекомендуется рассматривать его как ионное твердое вещество с ковалентным характером (характер связи до сих пор остается проблемой).
разложение
Сначала было упомянуто, что его образование является термодинамически обратимым, поэтому он поглощает тепло, чтобы вернуться в свое металлическое состояние. Все это можно выразить двумя химическими уравнениями для таких реакций:
Где Q представляет тепло в уравнении. Это объясняет, почему огонь, сжигающий поверхность ржавой серебряной чашки, возвращает свой серебристый блеск.
Поэтому трудно предположить, что существует Ag2O (l), так как оно мгновенно разлагается под воздействием тепла; если только давление не является слишком высоким для получения указанной коричневой черной жидкости.
номенклатура
Это потому, что ион Ag + является более распространенным, чем другие, поэтому Аг2Или как единственный оксид; что совсем не правильно.
Если вы считаете, Ag 2+ так как практически не существует, учитывая его нестабильность, то будут присутствовать только ионы с валентностями +1 и +3; то есть Ag (I) и Ag (III).
Валенсия I и III
Если Ag (III) полностью игнорируется, то его традиционная номенклатура должна быть: оксид серебра вместо оксида аргентина.
Если структура Ag наблюдается2О3, можно предположить, что это продукт окисления озоном, ИЛИ3, вместо кислорода. Следовательно, его ковалентный характер должен быть больше, поскольку он представляет собой ковалентное соединение со связями Ag-O-O-O-Ag или Ag-O.3-Ag.
Систематическая номенклатура сложных оксидов серебра
AgO, также написано как Ag4О4 или Ag2O ∙ Ag2О3, это оксид серебра (I, III), так как он имеет обе валентности +1 и +3. Его название в соответствии с систематической номенклатурой будет: тетраплат тетраоксид.
Эта номенклатура очень помогает, когда речь идет о других стехиометрически более сложных оксидах серебра. Например, предположим, что два твердых вещества 2Ag2O ∙ Ag2О3 и Ag2O ∙ 3Ag2О3.
Написание первого более подходящим способом будет следующим: Ag6О5 (считая и добавляя атомы Ag и O). Его имя тогда будет гексаплатной пятиокисью. Обратите внимание, что этот оксид имеет состав серебра менее богатый, чем Ag2О (6: 5
Серебро
Наиболее устойчивая степень окисления серебра в соединениях – +1.
Серебро стоит в электрохимическом ряду напряжений за водородом, поэтому не реагирует с растворами кислот не окислителей. Исключение – H2S в присутствии кислорода воздуха:
4Ag + 2H 2S + O 2 → 2Ag 2S + 2H 2O
С концентрированной серной кислотой :
2 Ag + 2H 2SO 4 → Ag 2 SO 4 + SO 2 ↑ + 2H 2O
С азотной кислотой :
Серебро реагирует с галогенами :
Но на свету галогениды разлагаются :
С серой при сплавлении:
2Ag + O 3 → Ag 2O + O 2
Полученный оксид разлагается при чуть большем нагревании, чем та температура, при которой серебро было окислено озоном:
2 Ag 2 O → 4 Ag + O 2
Ag2O – основный оксид:
Ag 2 O + 2 HNO 3 → 2 Ag NO 3 + H 2 O
С раствором аммиака образует комплексное соединение:
Аммиачный раствор оксида серебра используется в реакции серебряного зеркала:
И для определения строения алкинов (водород при тройной связи):
С перекисью водорода Ag +1 проявляет окислительные свойства:
Ag 2 O + H 2 O 2 → 2 Ag + H 2 O + O 2 ↑
Эта особенность связана с тем, что при растворении незначительных количеств малорастворимого оксида серебра в воде, среда раствора становится щелочной, а значит, оксид серебра в незначительной степени взаимодействует с водой с образованием достаточно сильного основания. AgOH существует только очень разбавленных растворах и легко разлагается на оксид и воду. Поэтому при написании реакций обмена солей серебра со щелочами следует записывать образование оксида серебра, а не его гидроксида, например:
2Ag NO 3 + 2NaOH → Ag 2O ↓ + 2NaNO 3 + H 2O