С чем реагирует оксид калия
Оксид калия
| Оксид калия | |
 | |
| Общие | |
|---|---|
| Химическая формула | K2O |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 94.20 г/моль |
| Плотность | 2.35 г/см³ |
| Термические свойства | |
| Температура плавления | 740 °C |
| Классификация | |
| Рег. номер CAS | 12136-45-7 |
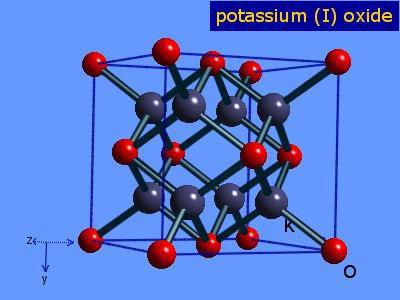
СодержаниеФизические свойстваОксид калия K2O — бледно-жёлтое, иногда бесцветное, редко встречающееся вещество. Содержится в некоторых видах удобрений и цемента. Химические свойстваПроизводствоОксид калия производят взаимодействием кислорода и калия, в результате реакции образуется пероксид калия, K2O2. Обогащением пероксида калием получают оксид: [2] Более удобным способом является нагревание нитрата калия с металлическим калием: Гидроксид калия не может быть обезвожен до оксида. См. такжеСсылкиПолезноеСмотреть что такое «Оксид калия» в других словарях:оксид калия — (K2O) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN potassium oxide … Справочник технического переводчика Оксид натрия — Оксид натрия бинарное неорганическое вещество, имеющее формулу и относящееся к классу основных оксидов. Оксид натрия … Википедия Оксид золота(III) — Общие … Википедия Оксид золота(I) — Общие Систематическое наименование Оксид золота(I) Традиционные названия Закись золота, окись золота Химическая формула Au2O Физические свойства Сост … Википедия Оксид марганца(IV) — Общие … Википедия Оксид хрома(VI) — Общие … Википедия Оксид золота(I,III) — Общие Систематическое наименование Оксид золота(I,III) Традиционные названия Окисел золота; аурат золота Химическая формула Au[AuO2] Рациональная формула AuO … Википедия Оксид меди(I) — Оксид меди(I) … Википедия Оксид платины(II) — Общие Систематическое наименование Оксид платины(II) Традиционные названия Окисел платины Химическая формула PtO Физические свойства Состояние ( … Википедия Оксид платины(III) — Общие Систематическое наименование Оксид платины(III) Традиционные названия Окисел платины Химическая формула Pt2O3 Физические свойства … Википедия Оксид калия: способы получения и химические свойстваОксид калия K2O — Бинарное неорганическое вещество . Белый, термически устойчивый. Относительная молекулярная масса Mr = 94,20; относительная плотность для тв. и ж. состояния d = 2,33; tпл = 740º C при избыточном давлении. Способ получения1. Оксид калия можно получить путем взаимодействия калия и гидроксида калия при 450º С, в результате образуется оксид калия и водород : 2K + 2KOH = 2K2O + H2 2. При взаимодействии надпероксида калия и калия при температуре 700º C и избыточном давлении образуется оксид калия: Химические свойства1. При разложении оксида калия образуется пероксид калия и калий, температура при этом должна быть 350–430º С: 2. Оксид калия взаимодействует со сложными веществами: K2O + 2HCl = 2KCl + H2O. 2.3. При взаимодействии калия с оксидами образуются соли. 2.3.1. Реагируя с углекислым газом при 400º C оксид калия образует карбонат калия: 2.3.2. При 150–200º C, в результате взаимодействия оксида калия, и оксидом азота (IV) образуются нитрат калия и нитрит калия: 2.3.3. Оксид калия взаимодействует с оксидом алюминия при 1000º С. При это образуется алюминат калия: Формула оксида калия (K2O), свойства, риски и использование / химияФизико-химические свойстваОксид калия — это желтоватые тетраэдрические кристаллы без характерного аромата (Национальный центр биотехнологической информации, 2017). Его внешний вид показан на рисунке 2 (американские элементы, С.Ф.). Соединение имеет молекулярную массу 94,2 г / моль и плотность 2,13 г / мл при 24 ° С. Он имеет температуру плавления 740 ° C, хотя начинает разлагаться при 300 ° C (Royal Society of Chemistry, 2015). Соединение устойчиво к нагреванию и растворим в этаноле и эфире. К2Или он кристаллизуется в структуре антифторита. По этой причине положения анионов и катионов меняются местами относительно их положений в CaF.2, с ионами калия, координированными до 4 оксидных ионов, и ионами оксида, скоординированными с 8 калиями. К2Или это основной оксид и бурно реагирует с водой с образованием едкого гидроксида калия. Он распух и поглощает воду из атмосферы, инициируя эту энергичную реакцию. Оксид калия обратимо окисляется до пероксида калия при 350 ° С, бурно реагирует с кислотами, такими как соляная кислота, с образованием солей калия в соответствии с реакцией: Соединение реагирует с диоксидом азота с образованием нитрата и нитрита калия при температуре от 150 до 200 ° C: Оксид калия реагирует при низких температурах с аммиаком с образованием амидов и гидроксида калия в соответствии с реакцией: ВидеоВзаимодействие с кислотамиСамый распространенный случай — оксид калия + серная кислота = сульфат калия + вода. Уравнение реакции выглядит таким образом: Из уравнения можно сделать вывод, что для получения 174 граммов сульфата калия и 18 граммов воды необходимо взять 94 грамма рассматриваемого оксида и 98 граммов серной кислоты. Похожим образом происходит химическое взаимодействие между рассматриваемым оксидом и азотной кислотой. При этом образуется нитрат калия и вода. Уравнение этой реакции можно записать следующим образом: Таким образом, из 188 граммов рассматриваемого оксида и 252 граммов азотной кислоты можно получить 404 грамма нитрата калия и 36 граммов воды. По такому же принципу рассматриваемый оксид может реагировать и с другими кислотами. В процессе этого будут образовываться другие соли и вода. Так, к примеру, при реакции этого оксида с фосфорной кислотой получается фосфат и вода, с хлоридной кислотой — хлорид и вода и так далее. Физические свойства оксида калия:
| ||||||
| Тип вещества | неорганическое | |||||
| Внешний вид | бесцветные (иногда бледно-желтый) кубические кристаллы | |||||
| Цвет | бесцветный, иногда – бледно-желтый | |||||
| Вкус | —* | |||||
| Запах | — | |||||
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество | |||||
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м 3 | 2320 | |||||
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см 3 | 2,32 | |||||
| Температура кипения, °C | — | |||||
| Температура плавления, °C | 740 | |||||
| Температура разложения, °C | 300 | |||||
| Гигроскопичность | высокая гигроскопичность | |||||
| Молярная масса, г/моль | 94,196 |
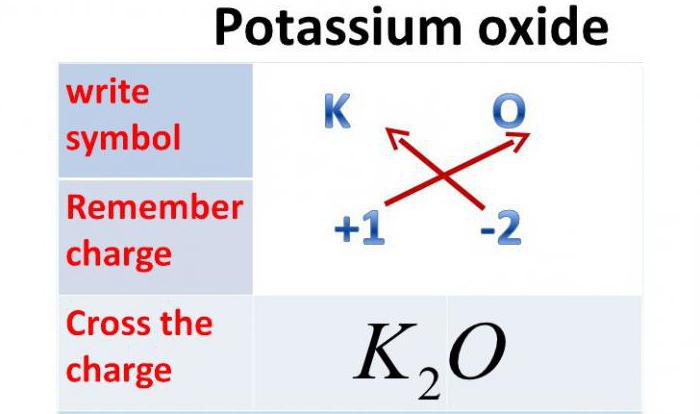
Оксид калия: формула
Так как валентность данного металла равна одному, а валентность кислорода — двум, то это химическое соединение будет состоять из двух атомов металла и одного атома Оксигена. Итак, оксид калия: формула — К2О.
Физические свойства основных оксидов:
Общим физическим свойством для всех основных оксидов является то, что они представляют собой твердые вещества. В то время как другие: внешний вид, цвет, плотность, температуры плавления и кипения, молярная масса, твердость и пр. различаются.
Оксид калия, характеристика, свойства и получение, химические реакции
Оксид калия, характеристика, свойства и получение, химические реакции.
Оксид калия – неорганическое вещество, имеет химическую формулу K2O.
Краткая характеристика оксида калия:
Оксид калия – неорганическое вещество бесцветного либо бледно-желтого цвета.
Так как валентность калия равна одному, то оксид калия содержит один атом кислорода и два атома калия.
Химическая формула оксида калия K2O.
В воде не растворяется, а вступает в реакцию с ней.
Растворим в органических растворителях.
Обладает высокой гигроскопичностью.
Физические свойства оксида калия:
| Наименование параметра: | Значение: |
| Химическая формула | K2O |
| Синонимы и названия иностранном языке | potassium oxide (англ.) |
калия окись (рус.)
Получение оксида калия:
Оксид калия получается в результате следующих химических реакций:
Вначале получают пероксид калия.
Затем пероксид калия обогащают калием.
Напрямую оксид калия путем окисления самого калия не получается.
Химические свойства оксида калия. Химические реакции оксида калия:
Химически активное вещество.
1. реакция оксида калия с галогенами:
Оксид калия бурно реагирует с галогенами, образуя соответственно две соли:
– хлорид калия и гипохлорит калия,
– бромид калия и гипобромит калия,
– йодид калия и гипойодит калия.
2. реакция оксида калия с водой:
3. реакция оксида калия с оксидом углерода (углекислым газом):
Оксид калия на воздухе реагирует с углекислым газом (являющийся кислотным оксидом), образуя соль – карбонат калия.
4. реакция оксида калия с оксидом серы:
Оксид серы также является кислотным оксидом. В результате реакции образуется соответственно соль – в первом случае – сульфит калия, во втором случае – сульфат калия.
5. реакция оксида калия с оксидом кремния:
Оксид кремния также является кислотным оксидом. В результате реакции образуется соль – силикат калия.
Аналогично проходят реакции оксида калия и с другими кислотными оксидами.
6. реакция оксида калия с оксидом цинка :
Оксид цинка является амфотерным оксидом. Это значит, что как амфотерный оксид оксид цинка проявляет свойства как кислотных, так и основных соединений. В результате реакции образуется соль – цинкат калия.
Аналогично проходят реакции оксида калия и с другими амфотерными оксидами.
7. реакция оксида калия с плавиковой кислотой:
В результате химической реакции получается соль – фторид калия и вода.
Аналогично проходят реакции оксида калия и с другими кислотами.
8. реакция оксида калия с бромистым водородом (бромоводородом):
9. реакция оксида калия с йодоводородом:
10. реакция оксида калия с жидким аммиаком:
В результате химической реакции получается гидроксид калия и амид калия.
Применение и использование оксида калия:
Примечание: © Фото //www.pexels.com, //pixabay.com
оксид калия реагирует кислота 1 2 3 4 5 вода
уравнение реакций соединения масса взаимодействие оксида калия
реакции с оксидом калия
Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Оксид калия: формула, взаимодействие
Что такое оксид?
Это соединение, состоящее из двух разных химических элементов, одним из которых является кислород. Вторым же может быть металл или неметалл. Количество атомов кислорода зависит от валентности второго химического элемента, входящего в состав соединения. Так, например, валентность калия равна одному, поэтому оксид калия будет содержать один атом кислорода и два атома калия. Валентность кальция равна двум, поэтому его оксид будет состоять из одного атома кислорода и одного атома кальция. Валентность фосфора равна пяти, поэтому его оксид состоит из двух атомов фосфора и пяти атомов кислорода.
Оксид калия: формула
Физические свойства
Рассматриваемый оксид обладает бледно-желтой окраской. Иногда он может быть и бесцветным. При комнатной температуре он обладает твердым агрегатным состоянием.
Температура плавления данного вещества равняется 740 градусам Цельсия.
При термическом разложении данного оксида образуется пероксид этого же металла и чистый калий.
Растворим в органических растворителях.
В воде не растворяется, а вступает в реакцию с ней.
Обладает высокой гигроскопичностью.
Химические свойства К2О
Данное вещество обладает типичными для всех основных оксидов химическими свойствами. Рассмотрим химические реакции данного оксида с различными веществами по порядку.
Реакция с водой
В первую очередь оно способно реагировать с водой с образованием в результате гидроксида данного металла.
Уравнение такой реакции выглядит следующим образом:
Зная молярную массу каждого из веществ, из уравнения можно сделать следующий вывод: из 94 граммов рассматриваемого оксида и 18 граммов воды можно получить 112 граммов калий гидроксида.
С другими оксидами
Уравнение реакции оксида калия и оксида карбона можно записать следующим образом:
Так, можно сделать вывод, что из 94 граммов рассматриваемого оксида и 44 граммов углекислого газа получается 138 граммов калий карбоната.
Взаимодействие оксида калия с оксидом сульфура можно выразить следующим уравнением:
Из него видно, что, взяв 94 грамма рассматриваемого оксида и 80 граммов оксида сульфура, можно получить 174 грамма сульфата калия.
Таким же образом К2О может реагировать и с другими оксидами.
Эту реакцию можно выразить следующим уравнением:
Из него видно, что при взаимодействии рассматриваемого оксида и оксида цинка образуется соль под названием калий цинкат. Если знать молярную массу всех веществ, то можно подсчитать, что из 94 граммов К2О и 81 грамма оксида цинка можно получить 175 граммов калий цинката.
Также К2О способен взаимодействовать с оксидом азота. При этом образуется смесь из двух солей: нитрата и нитрита калия. Уравнение этой реакции выглядит таким образом:
Если знать молярные массы веществ, можно сказать, что из 94 граммов рассматриваемого оксида и 92 граммов оксида нитрогена можно получить 101 грамм нитрата и 85 граммов нитрита.
Взаимодействие с кислотами
Из уравнения можно сделать вывод, что для получения 174 граммов сульфата калия и 18 граммов воды необходимо взять 94 грамма рассматриваемого оксида и 98 граммов серной кислоты.
Похожим образом происходит химическое взаимодействие между рассматриваемым оксидом и азотной кислотой. При этом образуется нитрат калия и вода. Уравнение этой реакции можно записать следующим образом:
Таким образом, из 188 граммов рассматриваемого оксида и 252 граммов азотной кислоты можно получить 404 грамма нитрата калия и 36 граммов воды.
К2О и галогены
Рассматриваемое химическое соединение способно реагировать и с веществами данной группы. К галогенам относятся простые соединения, состоящие из нескольких атомов одного и того же химического элемента. Это, например, хлор, бром, иод и некоторые другие.
Итак, хлор и оксид калия: уравнение:
В результате такого взаимодействия образуется две соли: хлорид и гипохлорит калия. Из 94 грамм рассматриваемого оксида и 70 грамм хлора получается 74 грамма хлорида калия и 90 грамм гипохлорита калия.
Взаимодействие с аммиаком
К2О способен реагировать с этим веществом. В результате такого химического взаимодействия образуется гидроксид и амид калия. Уравнение данной реакции выглядит следующим образом:
Зная молярные массы всех веществ, можно вычислить пропорции реагентов и продуктов реакции. Из 94 граммов рассматриваемого оксида и 17 граммов аммиака можно получить 56 граммов гидроксида калия и 55 граммов амида калия.
Взаимодействие с органическими веществами
Из органических химических веществ оксид калия взаимодействует с эфирами и спиртами. Однако эти реакции идут медленно и требуют специальных условий.
Получение К2О
Данное химическое вещество можно получать несолькими способами. Вот самые распространенные из них:
Использование К2О в промышленности
Наиболее часто рассматриваемое вещество используется в сельскохозяйственной промышленности. Данный оксид является одним из компонентов минеральных удобрений. Калий очень важен для растений, так как повышает их стойкость к различным заболеваниям. Также рассматриваемое вещество применяется в строительстве, так как может присутствовать в составе некоторых видов цемента. Кроме того, оно применяется в химической промышленности для получения других соединений калия.